制藥業是大企業,但通常不被認可的大部分是具有復雜供應鏈,精細化學工藝和產品且必須滿足嚴格質量控制要求的制造業。業內很少有人考慮如何安全,有效,大規模地以可靠的質量和精確計量的劑量來生產藥物。
更有趣的是,簡單的事實是,制藥廠經常使用已經過時數十年的制造工藝來生產復雜的藥物,并且在可比較的行業(例如化學制造)中正在逐步淘汰這種工藝。使用物聯網傳感器數據和預測性維護進行實時資產管理對于制藥行業的成功和革命至關重要。
批處理過程和過渡困難
藥品通常采用分批處理的方式生產,包括將化合物在大桶中混合,然后長時間拖延以測量每種中間產品的質量,然后進行下一步,有時在另一家工廠進行。機械不能連續使用。有關條件,狀態和質量的信息通常分布在各種各樣的獨立系統中。仍收集一些關鍵數據并將其存儲在紙質日志中。
如果制造過程是連續的,并用于從汽車到化學工業的各個方面,則制造效率會更高,在這種情況下,化合物可以不間斷地在工廠內移動,并經過測試和測量,從而發揮了物聯網的優勢。連續制造還可以更靈活地響應需求。如果需要更多,您可以運行更長的時間來逐步增加產品,而隨著批次的增加而增加數量則需要開始一個全新的批次,這意味著所有的延遲和供過于求的可能性。
不幸的是,在制藥業實現現代化生產工藝的途徑并非一帆風順。
法規驅動的行業
考慮到藥品制造中錯誤的可能后果,對藥品進行了嚴格的監管。這些法規幫助延遲了制造流程,現在將推動變革。
當美國食品藥品監督管理局(FDA)批準藥品時,批準的不僅是活性化合物。包括制造過程本身的詳細信息(包括工廠布局)。過程中的任何更改都需要獲得相關文件工作的明確監管批準。在其他行業中,持續的流程改進,更快的庫存訪問和步驟的取消是公司競爭優勢的一部分。制藥業轉型需要更多的計劃。
FDA已經認識到固有的監管困難,并成立了新興技術團隊(ETT),其目的是鼓勵采用新的制造方法,尤其是連續制造。目的是在任何法規提交之前,他們將在開發的早期與制藥公司會面。任何提議的制造過程都將在提交批準之前進行全面審查。
盡管FDA對全球藥品批準產生巨大影響,但它遠非唯一一家此類機構。全球有100多個藥品監管機構,全球制藥商在計劃更改生產流程時必須考慮到每個機構。
早期的成功
ETT已經證明了其有效性。自2015年以來,Vertex一直在為囊性纖維化藥物Orkambi使用連續生產。經過漫長的開發周期,Janssen(現為強生公司的一部分)于2016年轉向其HIV藥物Prezista的連續生產。兩者都與FDA密切互動,以確保在將藥物提交批準之前批準了制造過程。強生特別指出,結合以前由物聯網傳感器實現的單獨測試和采樣步驟是一項重大改進。
合規優勢
物聯網在合規性方面的優勢可能是其業務案例的重要組成部分,因為物聯網提供了監視和記錄制造過程中每個步驟的所有事件,變化和集中度的能力。從物聯網傳感器收集的數據使工廠操作員可以了解整個過程中發生的情況。如果某種化合物的特定運行與某種問題有關,這也可以為召回提供復雜的跟蹤。
物聯網還允許監視和記錄承包制造組織(CMO)的活動,這些活動執行大部分實際制造。藥物供應鏈變得越來越復雜,其中活性藥物成分(API)的制造,整體配方和包裝通常在不同的地方進行,通常由不同的簽約供應商進行。
因此,藥品監管機構對監控,跟蹤和報告的需求可以推動物聯網的采用并降低其速度。法規遵從性是經常被低估的IoT驅動程序。
物聯網與制藥業的發展之路
制藥設備及其組成成分往往非常昂貴,并且制造條件必須保持在極窄的公差范圍內。連續制造將使生產線上任何地方設備故障的后果更加嚴重。批處理可以在一個地方或另一個地方等待一會兒,這使得單點設備故障顯得更為寬容。使用物聯網傳感器數據和預測性維護進行實時資產管理至關重要。
除了停產線的成本外,還有保持質量的問題,這是FDA最重要的考慮因素。他們總是犯謹慎的一面,所以任何可能引起質量問題的藥物都是有罪的,直到被證明是無辜的。因此,預計故障,基于磨損的更換以及最少的計劃外停機時間將使管理制造質量,效率和法規遵從性變得更加容易,同時還能靈活地適應不斷變化的市場需求。
責任編輯:YYX
-
物聯網
+關注
關注
2910文章
44752瀏覽量
374588 -
FDA
+關注
關注
0文章
76瀏覽量
18338
發布評論請先 登錄
相關推薦
制劑車間物聯網系統建設方案


淺談安科瑞EMS2.0能效管理平臺在制藥廠潔凈室的電氣設計與選型
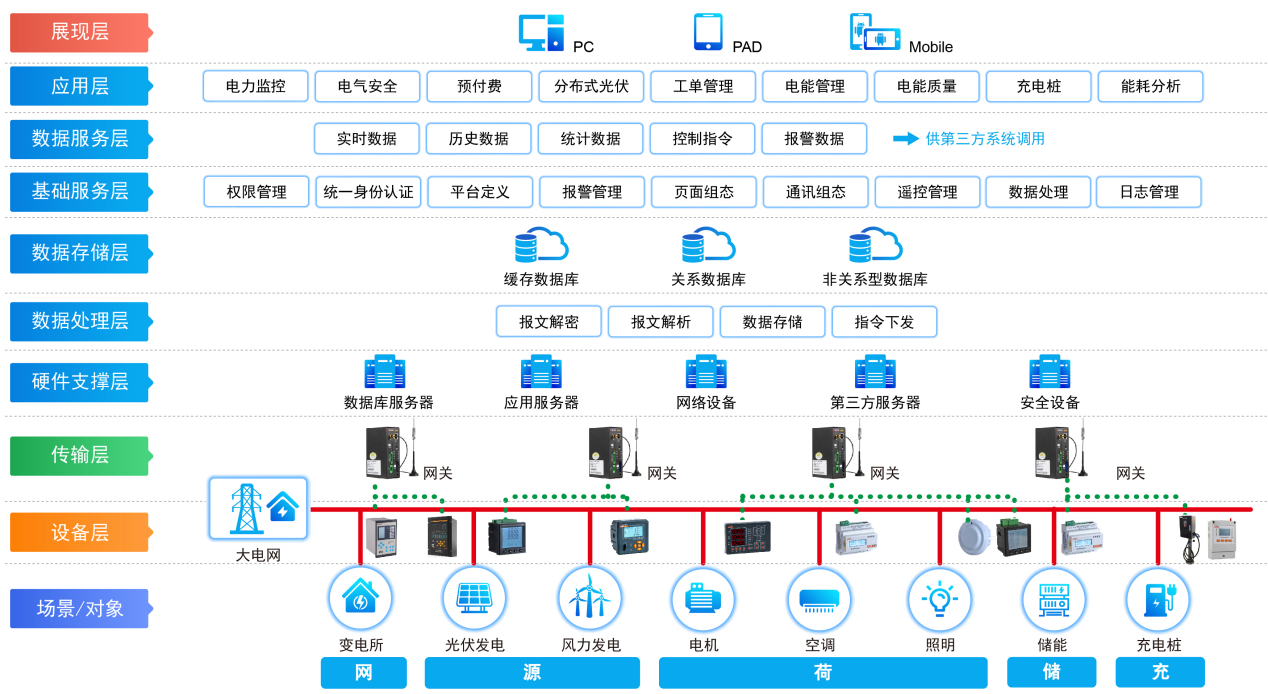
什么是物聯網技術?
2024:電梯物聯網的必然之路|梯云物聯
“物聯網+農業”助力農業節水增效高質量發展
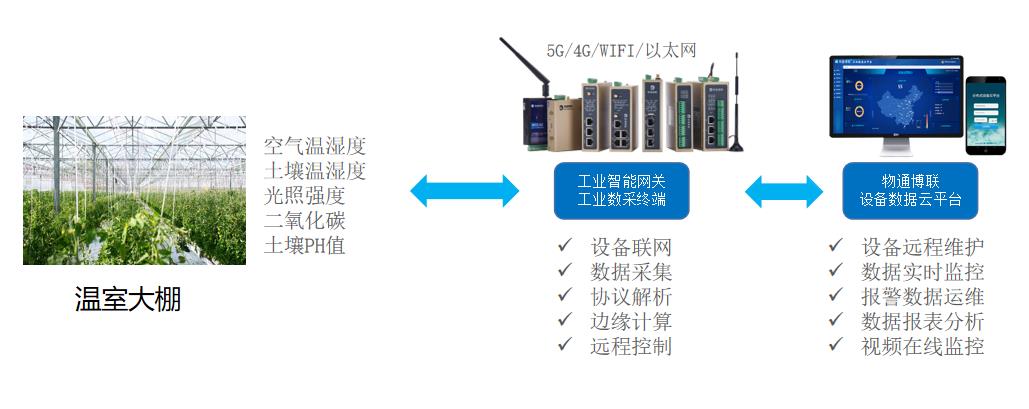
4G物聯網開關求助
以創新驅動農業可持續發展之路,共謀發展新篇張





 物聯網與制藥業的發展之路
物聯網與制藥業的發展之路










評論