近日,北京理工大學前沿交叉科學研究院黃淵余課題組在核酸藥物輸運和腫瘤免疫治療方面取得重要研究進展。該研究成果以《Rolling microneedle electrode array (RoMEA) empowered nucleic acid delivery and cancer immunotherapy》發表于納米科技與生物醫學領域國際頂級期刊《Nano Today》(影響因子16.907)。該論文第一作者為北京理工大學生命學院/前沿交叉院博士研究生楊同仁和北京大學黃東博士,通訊作者為北京理工大學黃淵余研究員和北京大學李志宏教授。 基于小干擾RNA(siRNA)的核酸藥物近年來連續獲批上市,已成為引領第三次制藥浪潮的代表性技術。siRNA藥物開發的關鍵問題是如何實現高效富集與胞吞、快速抵達細胞質、高效長效沉默靶基因表達,這個過程需要研究開發高效安全的藥物遞送技術。目前諸多遞送載體存在給藥效率低、安全性差、成本高、缺乏普適性等問題。
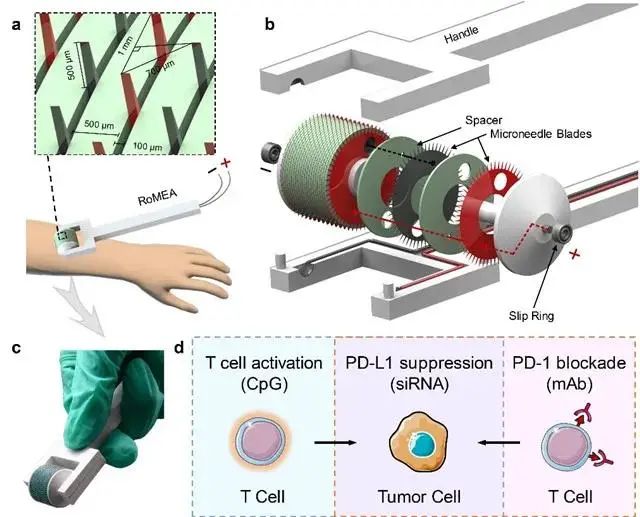
圖1 RoMEA示意圖及該研究思路 2018年,黃淵余課題組與李志宏課題組開展合作,提出并驗證了滾輪微針輔助柔性電穿孔芯片介導siRNA體內透皮遞送的策略(Theranostics 2018; 8(9):2361-2376),該策略結合醫療美容領域的微針滾輪與柔性插指電極芯片(FIEA),首先利用微針滾輪在小鼠皮膚組織建立微孔道、形成液體微電極,接著使用柔性電穿孔芯片給予脈沖電場,促使核酸藥物分子透皮遞送。進一步,研究人員構思將滾動式微針與電穿孔芯片“二合一”,設計了滾動式微針電極陣列(RoMEA,圖1),該器件的突出優勢在于滾動的同時施加同步電場,可支持在不規則的活體組織表面進行大面積的活體組織電穿孔。同時,該器件具有侵入性小、操作方便、安全、制造成本低、易于大規模生產等優點。
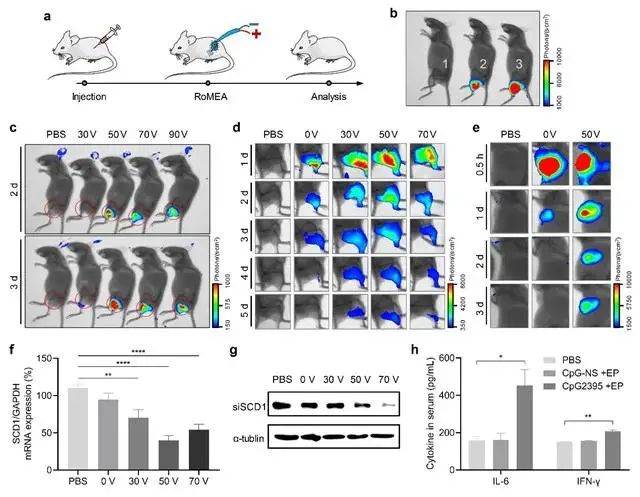
圖2 RoMEA介導的體內核酸遞送研究 研究人員通過RoMEA遞送表達紅色熒光蛋白(RFP)的質粒或Cy5標記的siRNA,或抑制SCD1基因表達的siRNA,對RoMEA在體內的核酸遞送的參數進行了探究(圖2)。結果顯示,當RoMEA所施加的電壓在30V-90V區間內,RFP的蛋白都得到顯著的表達,并且在50V的電壓下RFP的蛋白表達強度達到峰值(圖2c)。并且當RoMEA所施加的電壓為50V時,顯著的提高了Cy5-siRNA在小鼠腿部及腫瘤內的滯留時間(圖2d, e)。同樣,作者發現當RoMEA所施加的電壓為50V時siRNA有很好的基因抑制效率(圖2f, g)。在此條件下,電轉CpG2395(免疫佐劑)可以有效的刺激小鼠分泌IL-6與IFN-g(圖2h)。因此,RoMEA可以在50V的電壓下可以實現局部高效的核酸轉染效率。
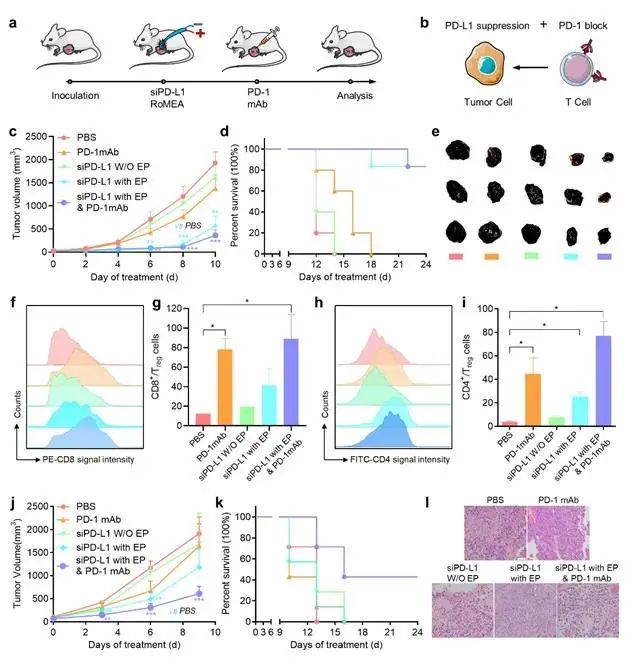
圖3 RoMEA介導的B16-F10黑色素瘤的免疫治療 阻斷PD-L1/PD-1免疫檢查點通路是臨床治療中最具代表性的腫瘤免疫治療途徑。結合RoMEA的最優參數,研究人員進一步選擇抑制PD-L1表達的siRNA(siPD-L1)和拮抗PD-1的單抗(PD-1 mAb)在B16-F10黑色素瘤小鼠模型進行研究(圖3a, b)。分別在腫瘤較小(模擬臨床早期腫瘤,圖3c-i)和腫瘤較大(模擬臨床中期腫瘤,圖3j-l)時開始治療。結果顯示,單獨使用siPD-L1或聯合PD-1 mAb,均能有效抑制腫瘤的生長,延長動物生存周期。同時,流式細胞術的結果顯示,腫瘤微環境中CD4+ T細胞、CD8+ T細胞數量顯著提升,證實了PD-L1/PD-1通路的機制和效果。 該工作設計的滾動式微針電極陣列(RoMEA)加工簡單、通用性強,為未來各種治療劑(不局限于核酸藥物)的應用開發奠定了基礎,展現了良好的實用前景。
責任編輯:lq
-
芯片
+關注
關注
456文章
51062瀏覽量
425806 -
生物醫學
+關注
關注
0文章
46瀏覽量
11176
原文標題:北理工在電穿孔介導核酸藥物免疫治療方面取得進展
文章出處:【微信號:MEMSensor,微信公眾號:MEMS】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
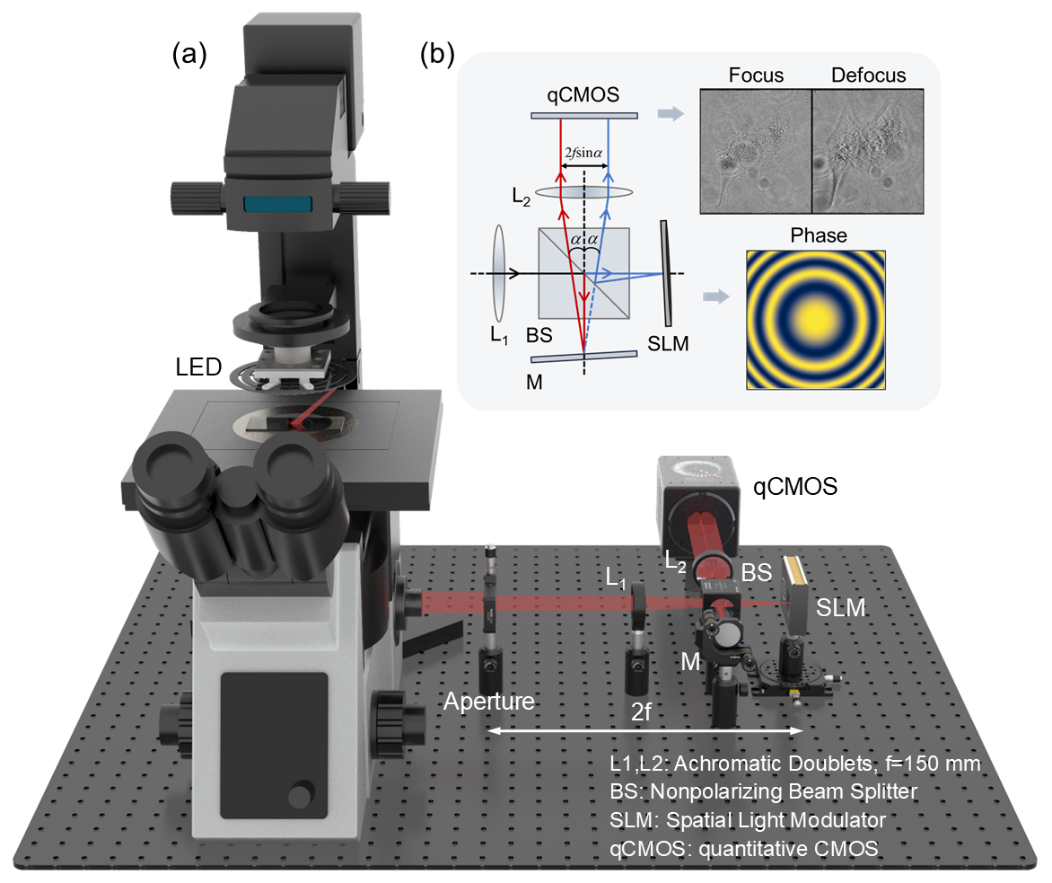
南京理工在計算光學顯微成像領域重要研究進展
使用原代腫瘤細胞進行藥物篩選的數字微流控系統
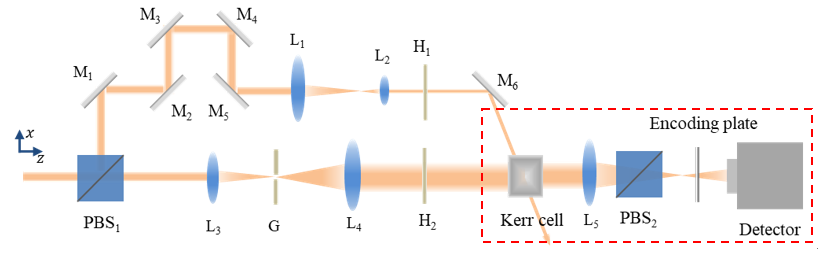
上海光機所在多路超短脈沖時空同步測量方面取得研究進展
AI大模型的最新研究進展
射頻功率放大器在腫瘤細胞表面EGFR研究中的應用
實戰分享:腫瘤電場治療硬件設計方案

哈爾濱工業大學在微納光學領域取得重要進展

天府錦城實驗室在生物傳感與蛋白質測序領域取得重要進展





 北理工在核酸藥物輸運和腫瘤免疫治療方面取得重要研究進展
北理工在核酸藥物輸運和腫瘤免疫治療方面取得重要研究進展














評論