基因療法作為一種可以實現治療性蛋白的長期表達和組織特異性表達的治療方法,可以實現治療傳統藥物不能治療的疾病,或大幅改善治療疾病的方式。甚至面對很多先天性遺傳的疾病時,基因療法是許多患者唯一的希望。
基因療法在技術上獲得實踐可能,離不開2012年CRISPR/Cas9技術的發現,“CRISPR”即“Clustered Regularly Interspaced Short Palindromic Repeats”,是細菌遺傳密碼及其免疫系統的一個定義性特征,是細菌用來保護自己免受病毒攻擊的防御系統。
實質上,它是一系列重復的DNA序列,并且這些DNA之間存在“spacers”。簡而言之,細菌利用這些基因序列來“記住”攻擊它們的每種病毒。細菌會將病毒的DNA整合到自己的細菌基因組中。這種病毒DNA最終成為CRISPR序列中的“spacers ”。這種防御系統可以在同種病毒再次發起攻擊時給予細菌保護或免疫力。
總是位于CRISPR附近的基因,稱為Cas(CRISPR相關)基因。一旦激活,這些基因就會產生特殊的蛋白質,這些蛋白質是與CRISPR共同進化的酶。這些Cas酶能夠充當切割DNA的“分子剪刀”。
簡單來說,當病毒侵入細菌時,其獨特的DNA會被整合到細菌基因組中的CRISPR序列中。這意味著下一次病毒攻擊時,細菌會記住它并發送RNA和Cas來定位和破壞病毒。
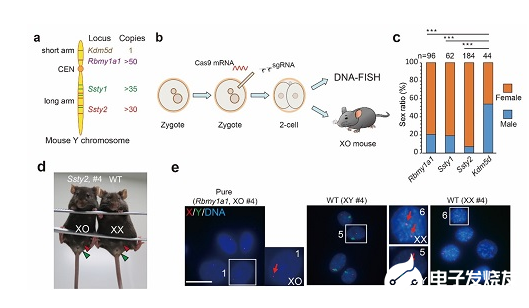
雖然細菌中還有其他Cas酶在病毒攻擊自己時會截斷病毒,但Cas9是動物體內執行這種任務的最佳酶。而CRISPR-Cas9就是指切割動物(和人類)DNA的Cas酶的種類。
因此,CRISPR/Cas9系統也被視為基因療法的剪刀。近日,約翰霍普金斯大學醫學院(Johns Hopkins Medicine)的研究人員,在一種常見細菌中,找到了CRISPR-Cas9系統工作原理的新線索,為開發新的Cas9工具帶來重要的指導意義。
和人類的免疫系統一樣,細菌的免疫系統也需要保持平衡:在識別和消除威脅時需要提高活性,同時要適時調低活性以便錯誤地攻擊細菌自己。其中,科學家們發現,CRISPR-Cas9系統中有一種RNA分子(tracrRNA),會導致該系統的活性急劇增加。這種tracrRNA分子像支架一樣,幫助Cas9攜帶向導RNA切斷特定的DNA序列。
tracrRNA有長、短兩種形式,它們結構相似,也都可以與Cas9結合。科學家們發揮CRISPR-Cas9的“基因剪刀”功能時,用的是短鏈tracrRNA。而在這項研究中,科學家們揭示了長鏈tracrRNA不曾被發現的功能。
研究人員發現,長鏈tracrRNA包含了一個模擬向導RNA的片段,但不同于向導RNA靶向病毒DNA序列,長鏈tracrRNA傾向于靶向CRISPR-Cas9系統本身。
而且,當它結合到特定位置時,并沒有讓Cas9剪切DNA,而是待在那里阻礙基因的表達。而當研究人員人為改變長鏈tracrRNA中某個區域的長度后,隨著長度的改變,Cas9可以恢復切割活性。
在另一組實驗中,研究人員培養了具有大量長鏈tracrRNA的細菌,CRISPR相關基因的表達量則非常低。而從中除去長鏈tracrRNA后,CRISPR-Cas9基因的表達量增加了100倍。
這意味著,長鏈tracrRNA其實是在抑制自身CRISPR相關的活性,而長鏈tracrRNA調節基因活動將為未來設計新型CRISPR-Cas9工具提供更多機會。
責任編輯:PSY
-
DNA
+關注
關注
0文章
243瀏覽量
31061 -
基因
+關注
關注
0文章
95瀏覽量
17221 -
免疫系統
+關注
關注
0文章
13瀏覽量
7304
發布評論請先 登錄
相關推薦
亞馬遜云科技發布Amazon Bedrock新功能
Amazon Q Business新功能發布,助力企業提效
Amazon Q Business發布新功能 助力企業提升內部工作效率
解析NVIDIA JetPack 6.1的新功能

首批Apple Intelligence功能驚艷亮相,12月新功能值得期待
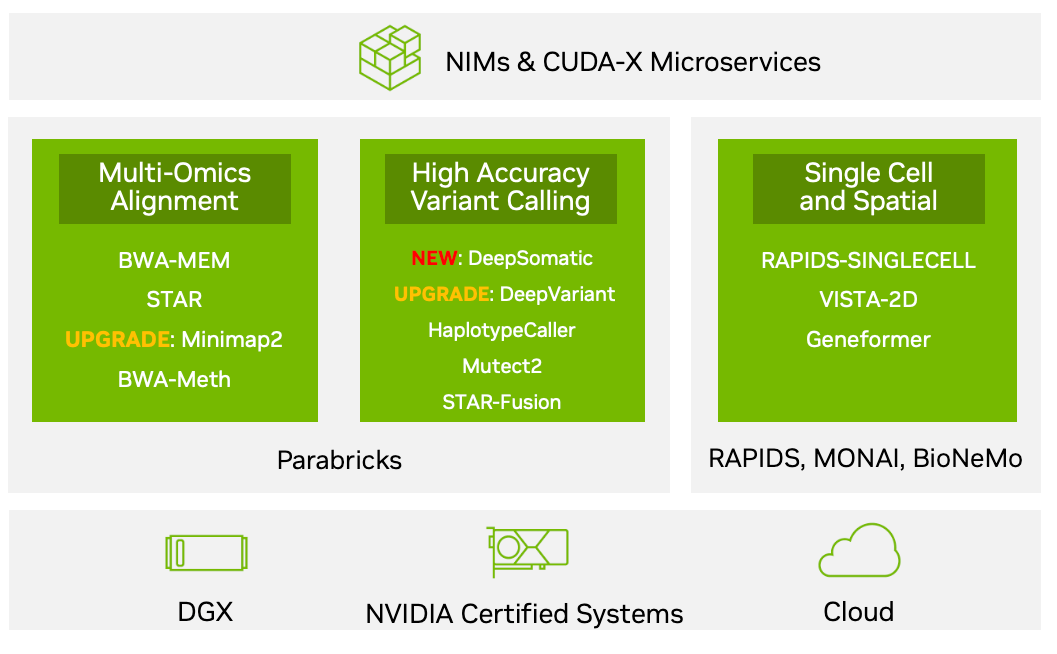
NVIDIA Parabricks v4.3.1版本的新功能
低功耗毫米波雷達解決方案使電池供電類接近感應產品實現新功能





 基因“剪刀”新功能 提供更多機會
基因“剪刀”新功能 提供更多機會










評論