近日,來自西南大學前沿交叉學科研究院生物學研究中心的夏慶友教授、林平研究員與陸軍軍醫大學陸軍特色醫學中心蔣建新院士、吳敏研究員合作在期刊Trends in Biotechnology上發表了題為“CRISPR-Cas-mediated diagnostics”的前瞻性綜述論文,全面系統總結了基于CRISPR-Cas技術的體外分子診斷研究取得的最新進展,詳細歸納了CRISPR診斷技術在不同領域的優勢,討論了CRISPR-Cas技術在未來臨床診斷中面臨的重大挑戰和問題及解決措施,并提出了“以實現CRISPR診斷技術自動化和一體化為紐帶聯系病患和醫院構建診療網絡”這一前瞻性策略。
CRISPR-Cas系統是細菌和古細菌內類人體免疫防御系統,靶向切割外源遺傳物質(DNA或RNA),實現抵抗外源病毒入侵。利用這一特點,將CRISPR-Cas系統開發為一種簡單、快速、經濟有效和精確的基因編輯技術,使基因診斷、病原防御和疾病治療發生了革命性的變化。
傳統診斷技術難以滿足需求
傳統PCR檢測技術是診斷各種傳染性疾病的主要手段。然而,以新型冠狀病毒(SARS-CoV-2)引發的新冠肺炎為例,基于PCR檢測技術的花費的時間為4-6小時,且檢測成本昂貴,依賴大型設備,使得在偏遠地區的醫療點難以開展檢測工作,同時存在感染早期呈現假陰性的等問題。基于抗原-抗體反應的檢測方法,如免疫熒光法、ELISA、免疫組化等技術,檢測呼吸道分泌物中的SARS-CoV-2抗原或血清抗體,同樣是SARS-CoV-2感染診斷或治療監測的輔助手段。但是免疫學檢測抗原或抗體存在交叉反應、檢測窗口期較長、假陽性率高等許多缺陷。在新冠疫情仍然全球大流行的背景下,如何有效快速診斷新型冠狀病毒感染者,降低傳染率和死亡率是目前亟待解決的問題。基于CRISPR-Cas系統的新一代基因編輯技術以其快速、便攜、經濟、高效的特點,為SARS-CoV-2的快速分子診斷提供了解決方案,可實現及早地追蹤和隔離被感染者,快速阻斷病毒傳播。論文對基于以CRISPR-Cas為基礎的新興診斷技術為病原微生物感染、癌癥等早期預防、分子診斷與治療監測的研究及其最新成果進行簡述。
CRISPR診斷技術的獨特優勢和不足
CRISPR-Cas系統由gRNA和Cas蛋白組成,現已經建立了基于Cas效應器(Cas9、Cas12、Cas13)的分子診斷體系(圖1)。主要通過采用等溫擴增技術擴增病原體的核酸序列,從而使CRISPR診斷方法的檢測速度超過傳統PCR,而且不依賴于樣本轉運、人員和大型PCR設備。CRISPR蛋白復合物對目標序列的準確識別確保了CRISPR系統的高靈敏度;隨后通過工具酶(例如Csm6)放大檢測信號、串聯使用gRNA以及引入微流控系統,將CRISPR系統的靈敏度提升至與PCR相似的水平。此外,CRISPR檢測方法本質上是試劑和樣品在一般條件下的混合反應,使得CRISPR診斷技術具備快速、靈敏、廉價、便攜、易操作的五大優勢。
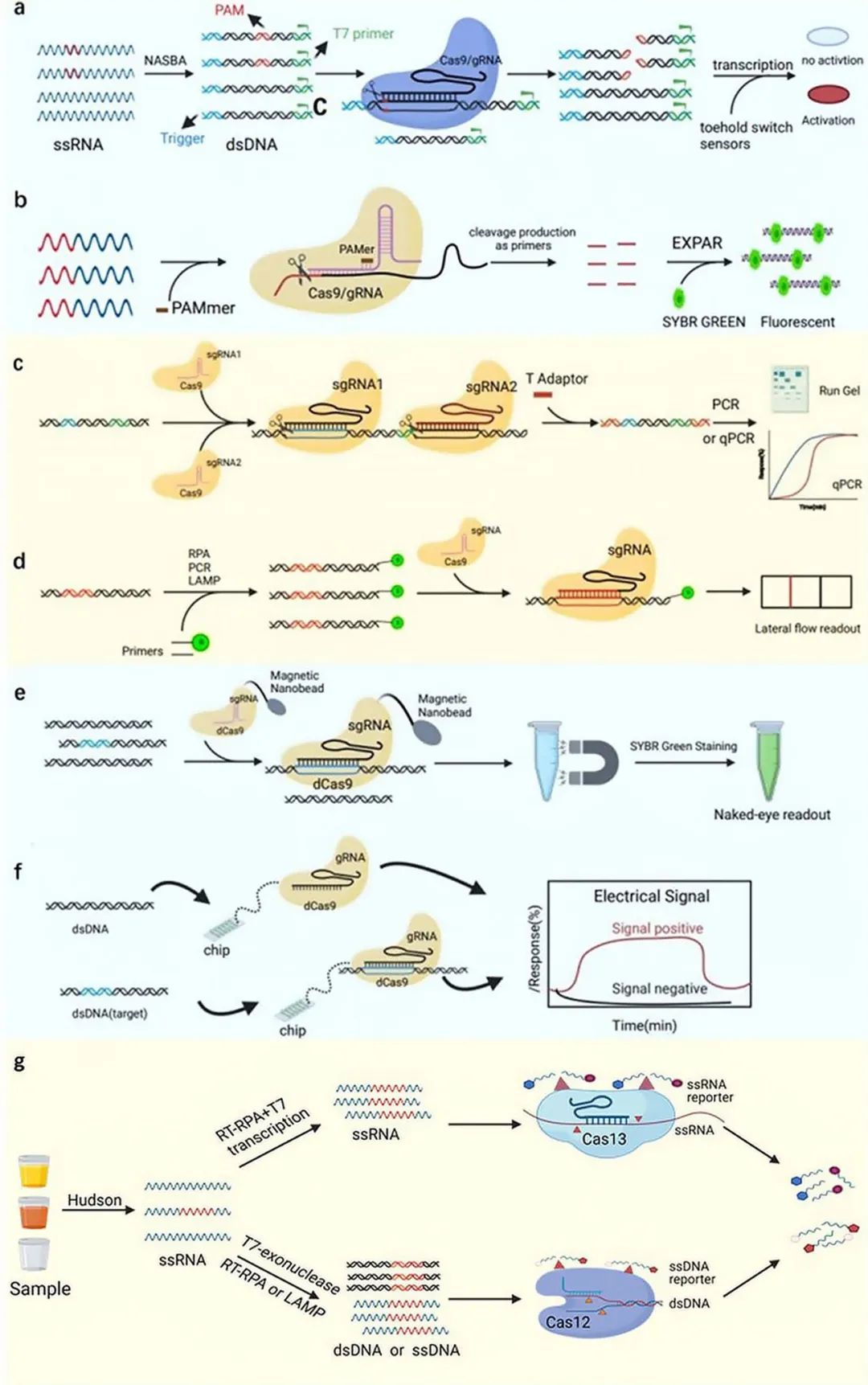
圖1 CRISPR診斷技術的流程圖:主要由樣本處理、預擴增、CRISPR檢測和結果讀數四部分組成
目前,Cas9蛋白介導的基因編輯技術研究最為成熟,容易與其他技術進行結合。Cas9介導的診斷體系主要是將Cas9蛋白作為一個檢測探頭與其他新興技術結合來提高檢測靈敏度或者衍生出檢測速度更快、成本更低的新方法,包括CAS-EXPAR技術、NASBACC技術、Cas9nAR、CASLFA等。而Cas12和Cas13蛋白利用靶向結合切割目標核酸的活性,同時附帶激活旁切活性(即非特異性切割DNA或RNA的酶切活性)。旁切活性能切割引入的核酸報告分子產生檢測信號,使CRISPR蛋白作為檢測體系的核心組件。論文總結了三種主要診斷體系的優勢、局限以及適用范圍(表1)。
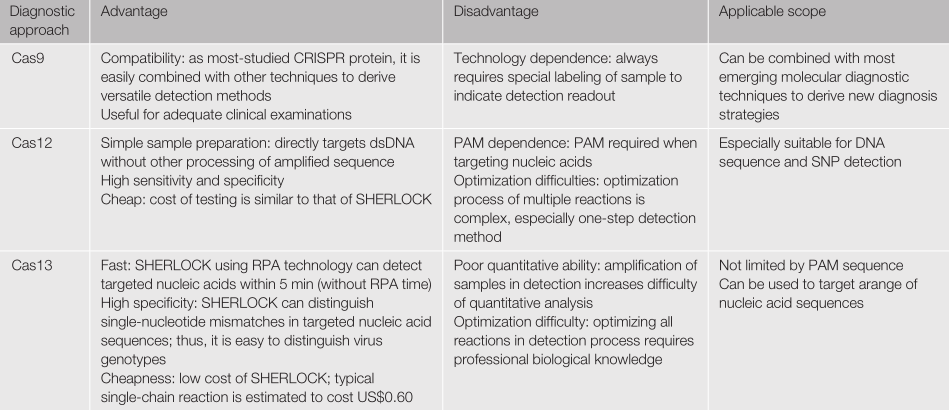
表1 CRISPR-Cas系統介導的分子診斷技術的優勢與不足
CRISPR系統給分子診斷帶來的革新
(1)核酸檢測
論文具體論述了各種CRISPR核酸技術(圖1)、闡述了基于CRISPR-Cas9系統的特異靶向DNA序列介導的檢測技術和基于CRISPR-Cas12/Cas13系統介導的旁切活性的檢測技術的原理、檢測性能、臨床應用情況。并且將針對特定病原體的CRISPR核酸檢測技術與PCR技術進行比較,從檢測周期、檢測性能、檢測成本、應用前景等方面對CRISPR技術進行綜合評估。基于Cas12、Cas13的核酸檢測技術更是將檢測時間縮短到1h以內,檢測成本最低可達到0.6美元/次。
同時,檢測體系的預擴增策略和讀數方式在近幾年不斷得到改進。擴增方式從RPA轉變為效率更高、特異性更強的LAMP方法。讀數方式由單一的顯微鏡讀取熒光信號到測流層析試紙讀數、比色法讀數、智能反應材料讀數等(圖2)。除此之外,微流控技術的引入也使多路復用的診斷策略得以實現。CARMEN-Cas13憑借微流控技術實現了在同一樣本中同時檢測169種病毒(圖3A)。這些新技術的引入使得CRIPSR技術的優勢能在核酸診斷領域更好的發揮。
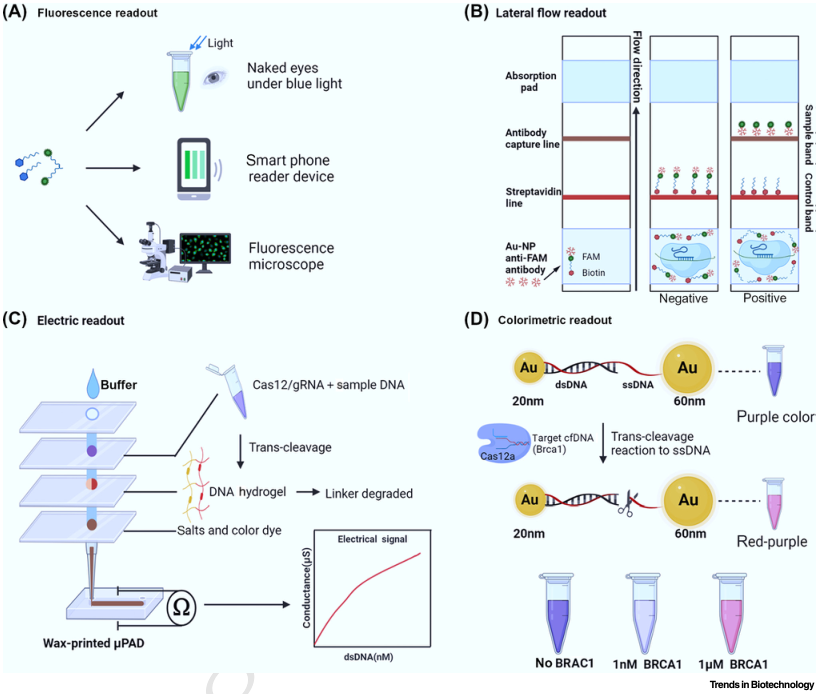
圖2 新興的讀數方法
(2)抗體診斷試驗
最近通過Cas9介導的自動組織技術(Cas9-mediated self-organization technology,PICASSO)開發了新的蛋白質微陣列構建方法。PICASSO將定制的多肽庫與dCas9蛋白融合表達,然后用單引導(Sg)RNA標記融合蛋白。融合蛋白可以自動組裝在包含數千個目標DNA的DNA微陣列上,以此構建蛋白質微陣列(圖3B)。這意味著特定的位置對應于特定的DNA和融合蛋白,這使研究人員能夠快速識別臨床樣本中的抗體或大規模研究各種感興趣的蛋白質。與傳統的蛋白質篩選工具相比,如噬菌體和核糖體展示,PICASSO可以實現蛋白質表達水平標準化以及蛋白結合可視化,這可以提高文庫篩選的代表性并且避免擴增偏差。
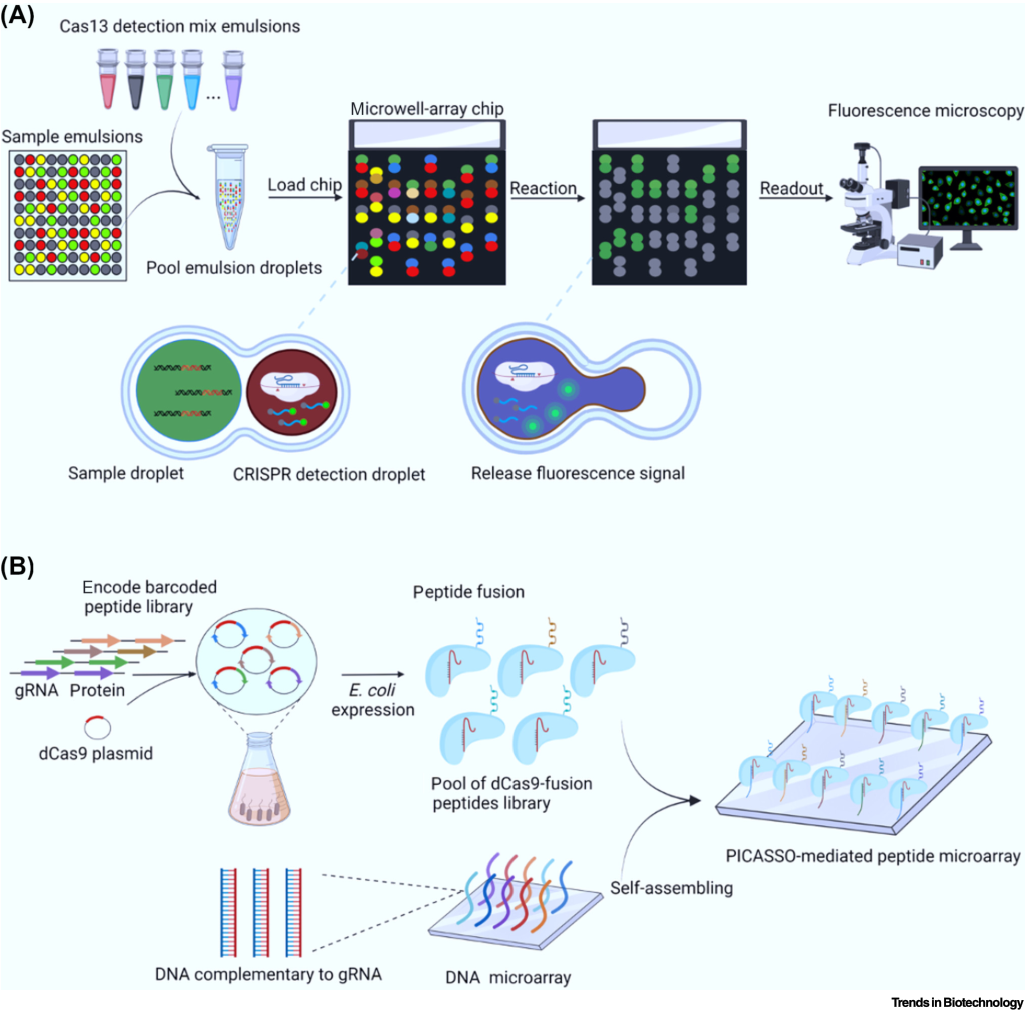
圖3 (A)CARMEN-Cas13微流控檢測方法原理圖; (B)PICASSO蛋白微陣列的組裝過程
(3)癌癥生物標志物檢測
癌癥相關生物標志物的檢測有助于癌癥患者的預后。CRISPR檢測技術可以檢測不同類型的癌癥生物標志物。與傳統的檢測方法如聚合酶鏈式反應和酶聯免疫吸附試驗相比,CRISPR檢測技術不需要昂貴的儀器和經驗豐富的操作員。例如,CRISPR技術可以檢測循環中的腫瘤DNA(ctDNA)和人體循環中的miRNA。Cas12a檢測系統可以在3小時內檢測到EGFR858和EGFR790,檢測限為0.005%。而蛋白質類型的生物標志物的檢測需要引入適配子。依據蛋白質的特殊結構設計相應適配子來靶向蛋白質,并且適配子結合目標蛋白后能被CRISPR系統檢測到,從而實現對蛋白質的檢測。目前基于CRISPR的蛋白質檢測方法有較高的靈敏度,但是由于適配子難以設計,該技術并沒有實現廣泛應用。
(4)CRISPR技術的發展前景
論文最后論述了“實現CRISPR診斷技術的自動化和一體化,并且以CRISPR診斷技術為紐帶聯系病患和醫院構建診療網絡”這一前瞻性策略(圖4)。目前通過優化和整合CRISPR診斷體系中的樣品處理、預擴增、CRISPR檢測和讀取過程,完全可能開發一體化CRIPSR檢測儀。而檢測自動化意味著降低檢測成本、加快檢測速度、統一診斷標準,這一舉措能夠擴大CRISPR診斷技術固有的優勢。診療網絡的構建不僅有利于對陽性人員進行及時處理,上傳的診斷數據還能夠指導CRIPSR檢測體系的進一步優化。
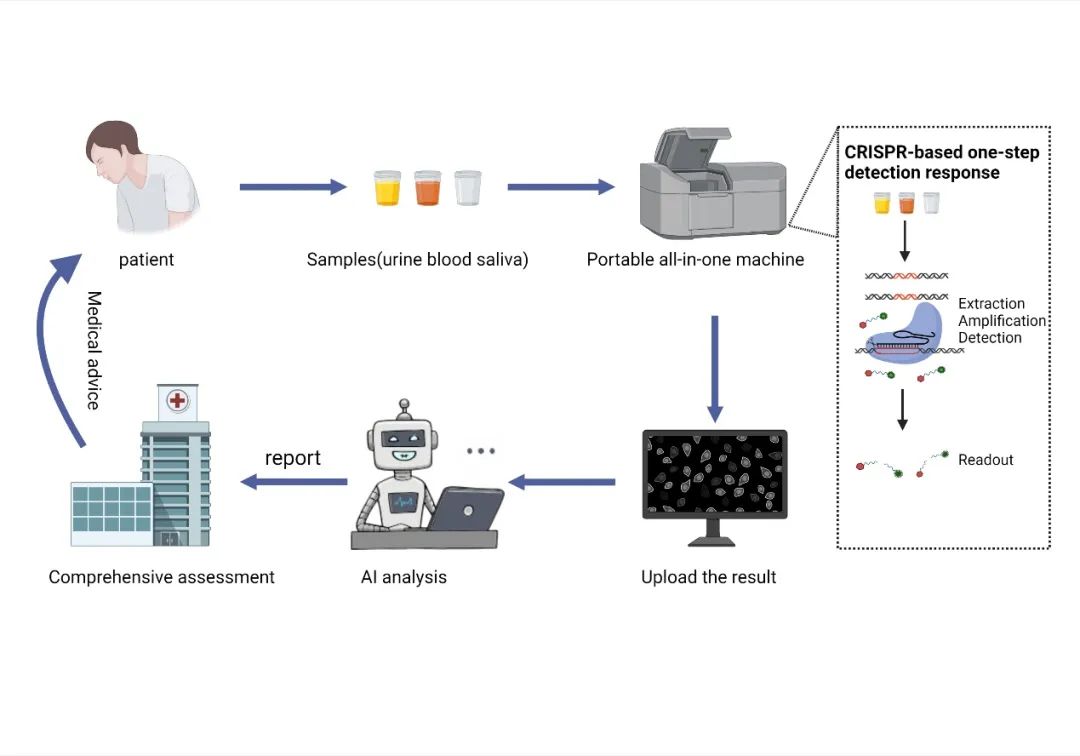
圖4 CRISPR診斷體系的前瞻性設想
-
檢測技術
+關注
關注
2文章
355瀏覽量
29077 -
PCR
+關注
關注
0文章
118瀏覽量
19593 -
微生物
+關注
關注
0文章
27瀏覽量
8878
原文標題:基于CRISPR-Cas系統的新一代分子診斷技術體系綜述
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
FPGA在自動駕駛領域有哪些優勢?
FPGA在圖像處理領域的優勢有哪些?
RFID技術在航空領域應用有什么優勢?
無線通信在應用中的優勢
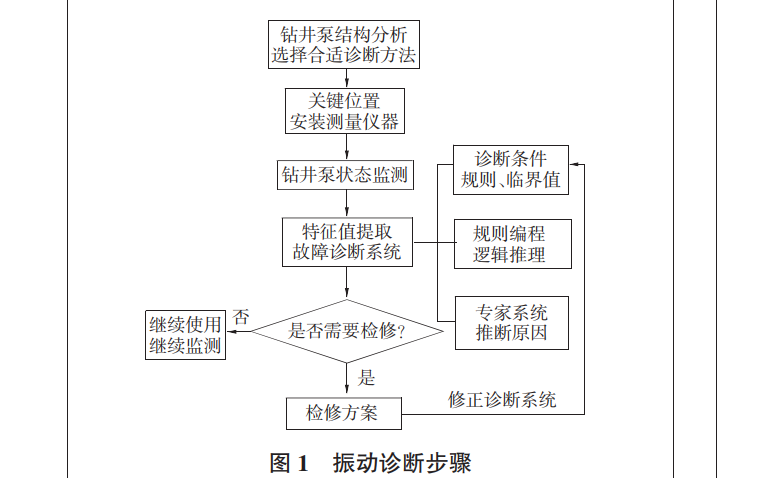
振動診斷技術在鉆井泵故障診斷中有怎么樣的作用和應用




 CRISPR診斷技術在不同領域的優勢
CRISPR診斷技術在不同領域的優勢










評論