熒光定量PCR(qPCR)是目前應用最廣泛的定量PCR技術,然而在接近單分子的核酸濃度下,qPCR的無法實現絕對定量,而更先進的數字PCR(dPCR)手段又存在成本高、耗時長、只能檢測低濃度樣本等限制。本文通過在硅基微流控芯片上進行PCR反應,討論了單分子的“原位擴增”現象的科學性和價值,利用原位擴增(在芯片上分子擴散局域化)現象實現了排除非特異性擴增、模板分辨和高靈敏度核酸檢測等應用。研究綜合了qPCR和dPCR兩者之長處,完成了ct值和絕對濃度之間的關聯,達到了從單分子等級到高濃度模板的超大濃度范圍分子檢測,對于快速精確定量未知濃度的核酸樣本提供了新的方法。
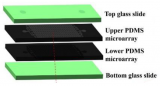
該團隊創新地使用了硅基微流控進行核酸擴增反應,利用高效帕爾貼技術、硅片隔熱設計和硅片的快速導熱特性,使得通常需要1-2小時的PCR反應在數分鐘內完成(圖1)。有趣的是,在模板濃度足夠低的情況下,微流控芯片內的核酸擴增并不均勻:部分流道區域有擴增現象,而有的區域完全沒有擴增。團隊將這種現象命名為“on-site PCR(osPCR),即原位擴增”現象(圖2)。
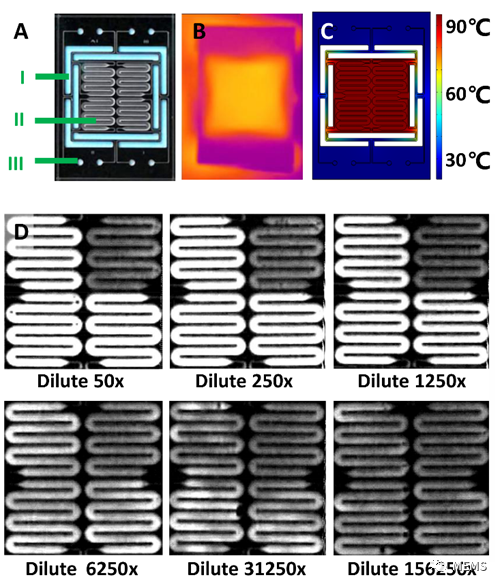
圖1 硅基微流控PCR系統(a)微流控芯片(b)加熱紅外圖(c)加熱熱學仿真(d)不同濃度模板擴增結果,每張圖右上角為陰性對照。
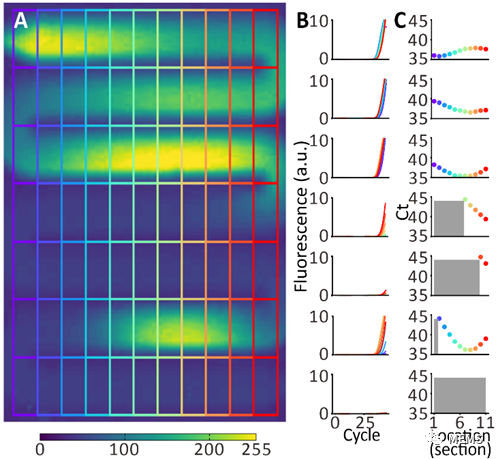
圖2 原位擴增現象分析(a)將不均勻流道拆分示意圖(b)每個拆分區域的熒光擴增信號(c)每個拆分區域的ct值,灰色代表沒有ct。
團隊對于osPCR現象進行了深入的研究,顯示“原位擴增”的點位來自于單個模板分子。團隊發現,原位擴增的點位數量和實際模板濃度正相關。對于同一芯片上,每一個擴增點位的ct基本一致,顯示其初始模板量一致。研究團隊假設大多數點位只有一個模板分子而計算出了相對應的模板濃度,該模板濃度與數字PCR得到的模板濃度吻合,證明了原位擴增現象可以像數字PCR一樣進行核酸的絕對定量(圖3)。
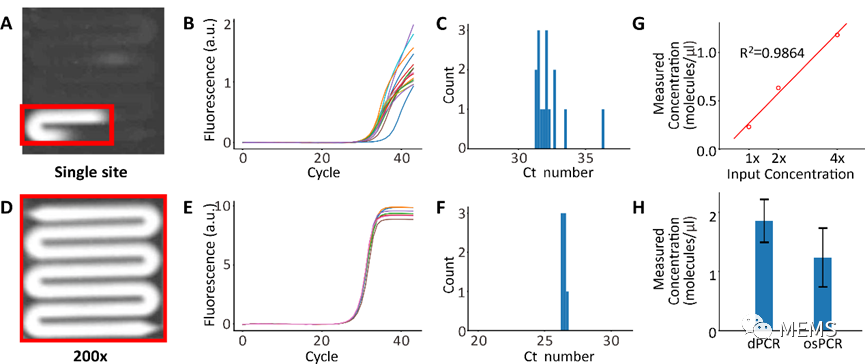
圖3 原位擴增來自單分子擴增(a-c)對于單個擴增點位的代表性照片(a)、擴增曲線(b)和ct分布(c) (d-f)對于均勻擴增流道的代表性照片(d)、擴增曲線(e)和ct分布(f)(g)原位擴增手段測試的模板濃度和實際濃度對比 (h)原位擴增手段測試的模板濃度和數字PCR測試濃度對比。
該研究團隊利用原位擴增現象首次實現了區分不同模板分子。團隊混合了兩種不同長度的模板同時擴增,原位擴增系統精準分辨出了不同的模板,并可以對各模板分別定量,甚至確認兩種模板的濃度比例(圖4)。利用這種對不同模板分子的區分能力,團隊展示了在低模板濃度時對非特異性擴增產物(如引物二聚體)的剔除。傳統qPCR在低模板濃度時容易出現由于副產物導致的ct值變化,而微流控系統可以剔除副產物信號,在有引物二聚體出現的時候,依然可以得到準確的ct值(圖5)。

圖4 利用原位擴增分辨模板(a)擴增圖片(b)熔解圖片(c)各點位擴增曲線圖(d)各點位熔解曲線原始圖和(e)各點位熔解曲線導數圖。
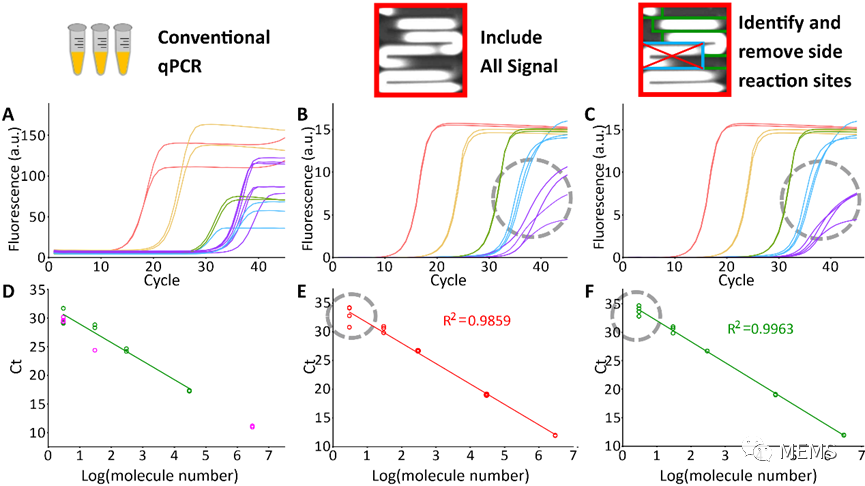
圖5 利用原位擴增去除副產物精確定量(a)不同濃度樣本傳統qPCR擴增曲線(b)不同濃度樣本原位PCR不剔除副產物擴增曲線(c)不同濃度樣本原位PCR剔除副產物擴增曲線(d-e)a-c的ct線型圖。
研究團隊將該系統應用于新冠臨床樣本檢測中,并針對性地開發了可以大幅度提升檢測靈敏度的滑窗算法。在新冠檢測中,微流控系統成功地檢出了所有傳統qPCR檢出的樣本(圖6)。更重要的是,在兩個傳統qPCR檢測結果模糊的樣本上,原位擴增系統都確認了樣本陽性,與臨床結果一致(表1)。因此,原位擴增系統有望在核酸檢測中作為傳統qPCR的擴展。
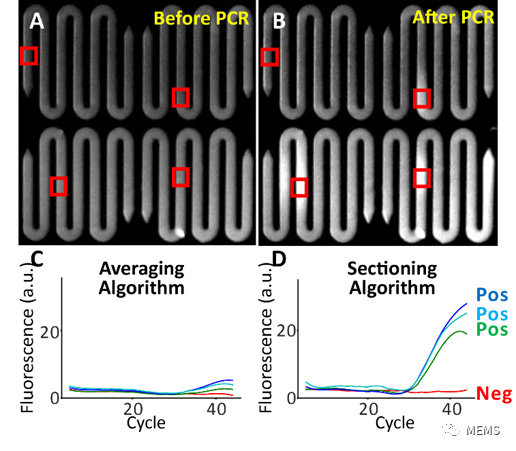
圖6 利用原為擴增進行臨床(a)PCR前照片(b)PCR后照片。紅色區域顯示滑窗算法關注位置。(c)使用傳統算法的擴增曲線和(d)使用滑窗算法的擴增曲線。
表1 傳統qPCR和原位擴增系統檢測效果對比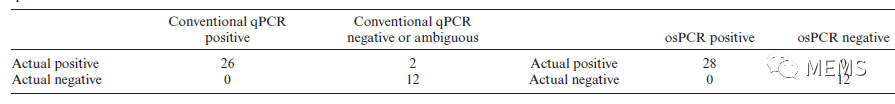
本文第一作者丁睿驊博士介紹道:“我們的技術將qPCR和dPCR進行了有機結合,將ct值對應的相對濃度和絕對模板數量進行了聯系。通過微流控的設計,我們不使用微孔或液滴手段也可以分離模板,達到數字PCR的效果。同時,對于每個擴增區域的分析使得我們可以有效剔除副產物,這使得我們的技術可以從根本上解決非特異性擴增在核酸定量中的影響,從而對于微量樣本達到更精確的定量。”
本文核心作者之一上海市實驗醫學研究院院長王華梁院長介紹道:“本方法的最大優勢主要是速度快,檢測線性范圍大,所以適合于任何需要檢測靈敏度高,快速出結果的場景。其中的原位擴增與以前的in situ的雜交反應是不同的,這個on site的技術凸顯的是PCR的過程,具有新的科學意義,也使得qPCR的反應體系能夠呈現出dPCR的效果。”
本文通訊作者田楨干主任介紹道:“相較于傳統手段,新技術檢測速度更快,同時具有更高的靈敏度,該項新技術的應用將極大地提升口岸的檢測效率。我們相信這種技術將會在未來持續發展,為我們的口岸現場快速檢測工作帶來更多的便利。”
本文通訊作者劉博博士介紹道:“本文是利用半導體芯片技術來實現超快PCR檢測,利用了芯片高加工精度、高可靠以及硅材料的高熱導性等特性。當芯片技術應用到生命科學研究課題中的時候,往往會有一些令人意想不到的驚喜,比如利用硅基核酸檢測芯片我們發現不光實現了快速核酸檢測,還由于硅基核酸芯片中分子擴散局域化的特征,在低拷貝數的情況下還能實現同數字PCR一樣的絕對定量,這也是信息技術同生物技術交叉融合所帶來新的發現,同時團隊在完成核酸檢測芯片研發過程中還打通了不同材料異質集成封裝的全鏈條。駟格生物作為一家致力于利用信息技術服務生命科學的創新型企業,將繼續深耕芯片微納制造領域,結合不同應用端未來還將帶來更多的創新產品和技術。”
本文通訊作者陳昌博士介紹道:“本文的工作是非常典型的生物與信息技術跨界融合的代表,我們將具有特殊熱學設計的微納硅基芯片應用在核酸擴增領域,不僅能實現生物反應的加速,而且還能額外實現單分子水平的不同靶標鑒定。同時,我們也是學術界和產業界的一個非常好的跨界合作,上海大學微電子學院的研究生、駟格生物的技術人員能夠在工研院和微系統所的產學研協同創新體系中得到成長,前沿技術能夠與現實應用充分結合。”
審核編輯:劉清
-
PCR
+關注
關注
0文章
118瀏覽量
19608 -
微流控系統
+關注
關注
1文章
77瀏覽量
1873
原文標題:?基于微流控的原位擴增助力核酸定量更快、更準、更細致
文章出處:【微信號:MEMSensor,微信公眾號:MEMS】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
常用的微流控芯片類型
ADS131A04使用外部基準Vref 5V和內部4V基準,如果5V精度是0.05%,轉換結果哪個更準?
固態光源點亮熒光原位雜交技術---提升生物醫學研究和臨床診斷新選擇


介紹一種用于絕對定量的微腔式數字PCR微流控芯片




 ?基于微流控的原位擴增助力核酸定量更快、更準、更細致
?基于微流控的原位擴增助力核酸定量更快、更準、更細致













評論