概述
全面的蛋白質序列和結構分析軟件,可與Nova蛋白質結構預測和建模工具集成。
找到一個集成了成功蛋白質分析所需所有組件的軟件包可能是一項挑戰。了解蛋白質的結構對于理解蛋白質的功能至關重要,但許多蛋白質分析工具忽略了蛋白質結構分析與蛋白質序列的生物物理特性之間的重要聯系。
LasergeneProtein 超越其他蛋白質分析工具,提供靈活、豐富的蛋白質結構3D圖形表示,與序列和結構分析完全集成,蛋白質設計工具可讓您輕松預測蛋白質穩定性,并通過集成預測蛋白質結構具有無與倫比的準確性使用我們的 Nova應用程序。
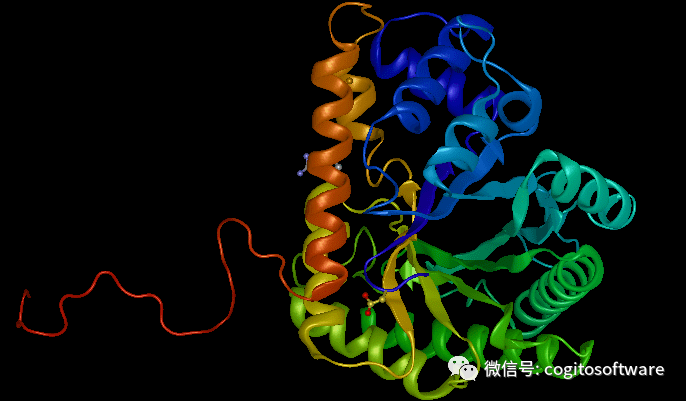
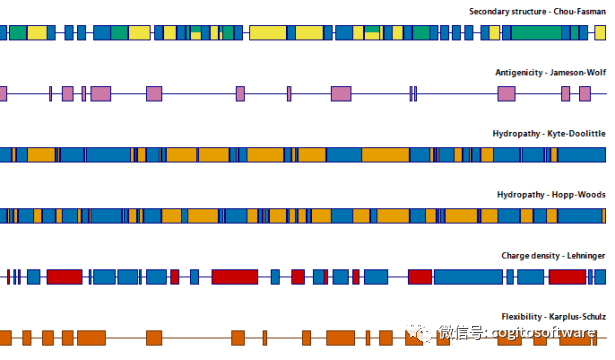
LasergeneProtein 工作流程
抗體建模*
使用NovaFoldAntibody 在幾分鐘內根據序列數據預測高度準確的抗體模型。
抗體建模是抗體設計和優化的重要工具,準確性至關重要。許多抗體建模工具僅依賴于同源建模,但 NovaFoldAntibody的獨特算法通過結合框架區的同源建模和基于片段或高變環區域的從頭建模來生成抗體和抗體片段的模型,從而實現高度準確的抗體結構預測。只需提供輕鏈、重鏈或兩者的序列,NovaFoldAntibody 將返回一份帶注釋的報告,其中包括預測的抗體模型、最高可能性的重鏈和輕鏈模板以及CDR環位置的注釋。通過 Protean3D(LasergeneProtein 的一部分)中的注釋輕松查看抗體建模結果,它允許您完全自定義渲染以幫助可視化,或準備要導出的出版質量圖像。使用 NovaFoldAntibody 進行的抗體建模也可以與NovaDock結合使用,以預測抗體-抗原復合物的結構和結合。
表位預測
使用Protean3D 僅使用基于序列的信息即可準確執行B細胞表位預測。
B細胞表位(抗體識別的抗原的一部分)本質上是構象的;然而,對于沒有已知 3D結構的蛋白質來說,準確的表位預測是困難的。Protean3D 是LasergeneProtein 的一部分,它采用機器學習方法,提高了僅使用基于序列的信息執行B細胞表位預測的能力,與其他領先的表位預測方法相比,提供了更好的整體預測準確性。Protean3D 使您能夠查看序列和結構上的預測表位和抗原區域,并將預測與其他特征(例如表面概率)進行比較。輕松在結構周圍創建分子和溶劑可及的表面,查看相對于蛋白質表面的預測表位,查看預測抗原區域的置信度分數,并更改序列和結構上預測表位的外觀,以優化可視化和出版質量的圖像。
蛋白質對接*
NovaDock探索對接時蛋白質的靈活性,從而實現更準確的蛋白質-蛋白質相互作用預測。
對蛋白質-蛋白質對接相互作用進行建模通常比預測單個蛋白質的結構更困難,并且由于其復雜性,準確性可能是一個問題。NovaDock能夠利用SwarmDock(CAPRI盲對接實驗中驗證的頂級算法之一)預測任意兩個結合伙伴的蛋白質-蛋白質對接相互作用。NovaDock利用SwarmDock算法探索對接時蛋白質的靈活性,從而實現更準確的預測。只需提供您的配體和受體 PDB或結構文件,并在需要時提出結合配偶體之間的特定殘基接觸。然后,NovaDock將預測多蛋白復合物的三維結構,并為每個模型提供能量評分、簇大小和配體接觸數量以供分析。
蛋白質序列分析
在一款易于使用的應用程序中使用Protean3D 進行全面的蛋白質序列分析!
蛋白質序列分析對于研究和預測蛋白質功能和結構至關重要,但蛋白質序列分析工具通常缺乏解釋所需的可視化組件,或者需要額外的工具進行下游分析。Protean3D 中提供的蛋白質序列分析工具提供了所應用方法的優雅圖形表示,使分析生物物理特性、預測B細胞表位等二級結構、計算表面概率、執行氨基酸組成分析等變得簡單。更重要的是,Protean3D是一個完整的蛋白質序列分析軟件包,這意味著在分析和注釋蛋白質序列后,您可以立即進行蛋白質結構分析,以及預測蛋白質結構、進行抗體建模或評估蛋白質-蛋白質對接互動。使用 Protean3D 在一款易于使用的應用程序中提供全面蛋白質序列分析所需的一切!
蛋白質穩定性預測
使用LasergeneProtein 的蛋白質設計軟件在幾分鐘內即可執行基本的蛋白質穩定性預測。
蛋白質穩定性預測對于優化蛋白質功能研究至關重要,但許多提高溶解度和表達的標準方法通常由于降解或熱力學不穩定而無效。我們的蛋白質設計軟件是 LasergeneProtein 的一部分,包括蛋白質突變穩定性預測工具,該工具使用確定性蛋白質設計算法來查找全局最小能量構象(GMEC)。這使您可以在蛋白質結構的殘基水平上進行改變,并預測與原始結構相比這些改變是否可能穩定或不穩定,這是PCR定點誘變的有益過程。我們的蛋白質穩定性預測工具還可以通過執行計算丙氨酸掃描或絲氨酸掃描來檢測熱點、其變體破壞結構穩定性的殘基,從而輕松搜索對蛋白質穩定性重要的氨基酸位置。使用 LasergeneProtein 的先進蛋白質設計軟件可在幾分鐘內進行準確的蛋白質穩定性預測!
蛋白質結構比對
使用Protean3D 輕松執行整個大分子結構或選定區域的蛋白質結構比對。
同源蛋白質通常具有相似的結構。蛋白質結構比對軟件可以成為通過比較結構之間的形狀和3D構象來識別這些相似性的有價值的工具。蛋白質結構比對也是將 NovaFold預測模型與蛋白質數據庫中的模板結構進行比較的寶貴工具。Protean3D 是LasergeneProtein 的一部分,可以輕松識別兩個或多個結構之間的相似區域,而與序列相似性無關。只需添加結構文件或打開 NovaFold結果,然后從TM-Align或jFATCAT剛體對齊算法中進行選擇。在進行蛋白質結構比對后,評估比對結構的 RMSD值,以確定它們之間的差異。然后,在 Protean3D 中自定義可視化的渲染,以準備要發布的蛋白質結構比對圖像。
蛋白質結構分析
在一款用戶友好的應用程序中使用Protean3D 進行完整的蛋白質結構分析!
了解蛋白質的結構對于理解蛋白質的功能至關重要,但當今可用的許多蛋白質結構分析工具缺乏有效分析所需的高質量可視化組件,并且錯過了蛋白質結構分析與蛋白質序列的生物物理特性之間的關鍵聯系。Protean3D 是LasergeneProtein的一部分,它通過創建美觀、靈活、豐富的蛋白質圖形表示并在單個應用程序中提供與蛋白質序列分析和結構預測工具的完全集成來消除這些挑戰。我們的蛋白質結構分析工具可以輕松分析您感興趣的蛋白質結構或引入突變并查看對蛋白質結構的影響。三維蛋白質結構可視化的無限可能性提供了一種生成出版質量圖像的簡單方法。使用 Protean3D 在一款用戶友好的應用程序中提供全面蛋白質結構分析所需的一切!
蛋白質結構預測*
創建高度準確的蛋白質模型,這是通過標準建模方法無法實現的。
根據獨特的氨基酸序列預測蛋白質3D結構非常重要,因為擁有蛋白質結構模型可以更好地理解蛋白質的工作原理,這可以讓我們創建關于如何影響它、控制它或修改它的假設。許多蛋白質結構預測工具僅依賴于同源建模,這僅適用于與蛋白質數據庫中的蛋白質序列具有高度序列相似性的蛋白質。
相比之下,NovaFold和NovaFoldAI 使用兩種不同的獲獎算法來創建高精度、完整的蛋白質3D原子模型,這是通過標準建模方法無法實現的。
-
NovaFold利用屢獲殊榮的I-TASSER蛋白質結構預測算法,該算法結合了線程和從頭開始折疊技術。NovaFold比單獨的序列相似性發現更遠的關系,從而提高了預測結構的質量和準確性。
-
NovaFoldAI 使用DeepMind(最近CASP14挑戰賽的獲勝者)的AlphaFold2 算法來預測距離并使用深度多序列比對作為輸入來創建二面體圖。該算法不直接使用模板來放置原子坐標,但可以使用模板作為地圖構建過程的一部分。
LasergeneProtein 應用程序
Protean3D
蛋白質序列和結構分析
Protean3D 提供靈活、豐富的蛋白質結構3D圖形表示,結合了序列和結構分析以及蛋白質穩定性預測工具。
NovaFold*
蛋白質結構預測
NovaFold是蛋白質結構預測軟件,可與LasergeneProtein 配合使用,為具有先前未知結構的蛋白質構建準確、完整的3D原子模型。
NovaFoldAntibody*
抗體建模
NovaFoldAntibody 軟件利用同源建模和從頭開始循環預測的組合生成高度準確的抗體和抗體片段模型。
NovaDock*
蛋白質-蛋白質對接
NovaDock是一款高分辨率蛋白質-蛋白質對接應用程序,可預測任意兩種蛋白質之間的原子相互作用。
對比DNASTARLasergene 軟件包
|
LasergeneMolecular Biology |
LasergeneGenomics |
LasergeneProtein |
DNASTARLasergene (最受歡迎) |
|
|
包含的應用程序 |
||||
|
SeqBuilderPro |
|
|
||
|
SeqManUltra |
|
|
|
|
|
MegAlignPro |
|
|
||
|
GeneQuest |
|
|
||
|
GenVision |
|
|
||
|
SeqNinja |
|
|
||
|
SeqManNGen |
|
|
||
|
ArrayStar |
|
|
||
|
GenVisionPro |
|
|
||
|
Protean3D (每個Nova應用程序+1預測) |
|
|
||
|
DNASTARNavigator |
|
|
|
|
-
模型
+關注
關注
1文章
3243瀏覽量
48842 -
應用程序
+關注
關注
37文章
3268瀏覽量
57710 -
蛋白質
+關注
關注
0文章
25瀏覽量
7984
原文標題:DNASTAR Lasergene Protein
文章出處:【微信號:哲想軟件,微信公眾號:哲想軟件】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦




 LasergeneProtein工作流程
LasergeneProtein工作流程










評論