腫瘤已成為全球人口死亡的主要原因,嚴重威脅著人類的生命健康。免疫治療是一種新興的抗腫瘤手段,其通過激活或增強自身免疫系統來識別和摧毀腫瘤細胞,在腫瘤治療方面具有巨大潛力。目前,常用的腫瘤免疫療法包括治療性腫瘤疫苗療法、單克隆抗體免疫療法、免疫檢查點抑制療法和過繼細胞療法等。治療性腫瘤疫苗療法在腫瘤免疫治療中占有重要地位,能夠誘導并放大腫瘤抗原的免疫反應,特異性地殺傷腫瘤細胞。微針系統是一種微創無痛的經皮給藥方式,可以穿過角質層將腫瘤抗原遞送至皮膚內特定深度并發揮特異性免疫反應,具有患者依從性高、給藥方便、儲運方便等優點。
據麥姆斯咨詢報道,近期,來自山東大學的研究人員在《中國藥學雜志》發表了題為“微針系統在腫瘤疫苗中的研究進展”的綜述文章,介紹了微針系統及其遞送腫瘤抗原的機制,并總結了微針系統遞送腫瘤抗原的研究進展,以期探索腫瘤抗原遞送的新途徑,推進微針系統在腫瘤疫苗中的應用,為新型腫瘤疫苗的開發提供參考。
微針系統應用于腫瘤疫苗中展現了其獨特的優勢:(1)能夠實現腫瘤抗原和佐劑的聯合遞送,誘導更高效的免疫應答;(2)能夠準確將腫瘤抗原與佐劑遞送至活性表皮和真皮層,直接且有效地作用于皮膚層的抗原遞呈細胞,快速啟動特異性免疫應答;(3)將腫瘤抗原封裝于微針中可以提高其穩定性,避免冷鏈儲存和運輸的不便性,降低儲運的成本;(4)微針的體積較小,給藥方便,無需專業人員操作就可以達到無痛給藥目的,大大提高患者的依從性。
微針穿透角質層后,釋放腫瘤抗原至活性表皮或真皮層,然后被活性表皮中朗格漢斯細胞(LC)和真皮中真皮樹突狀細胞(DDC)捕獲和提呈,促進樹突狀細胞(DC)活化并上調主要組織相容性復合體和共刺激分子B7表達,遷移并引流至淋巴結與T細胞表面受體結合,在共刺激分子和細胞因子作用下,T細胞完全活化并進一步增殖和分化,激活機體抗腫瘤免疫應答,有效發揮治療效果并獲得免疫記憶(圖1)。根據腫瘤疫苗微針中抗原的狀態,疫苗微針主要可分為游離抗原微針、納米疫苗微針和樹突狀細胞疫苗微針。
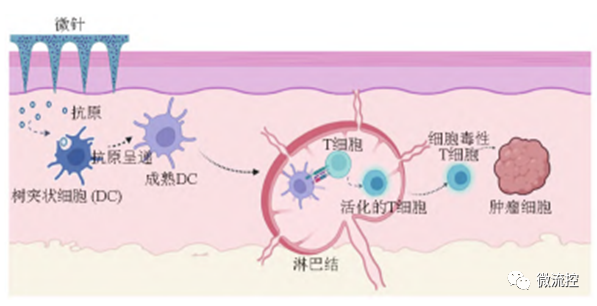
圖1 微針遞送腫瘤抗原作用機制
游離抗原微針
微針具有足夠的內部空間和表面積,可以將腫瘤抗原直接封裝在微針內部或涂覆在微針表面,實現游離抗原與佐劑有效遞送,發揮免疫治療療效。
(1)內部封裝游離抗原微針
將游離抗原與佐劑直接分散或溶解在微針的基質材料中,可直接制備水凝膠微針和可溶性微針。制備方法簡單易行,無需特殊設備與操作工藝。該類微針系統遞送的腫瘤抗原主要是蛋白/肽疫苗或細胞裂解物,基質材料常常選擇殼聚糖(CS)、透明質酸(HA)、聚乙烯吡咯烷酮(PVP)和聚乙烯醇(PVA)等。Ye等選擇基質為透明質酸的微針封裝黑色素腫瘤裂解物和粒細胞-巨噬細胞集落刺激因子,該微針系統巧妙地借助腫瘤裂解物中現有的天然色素,實現光熱治療,利于細胞因子的釋放和血液、淋巴液流量的增加,從而促進樹突狀細胞等免疫細胞遷移,最終啟動特異性免疫反應,誘導腫瘤的消退,為后續微針系統與其他療法的聯合應用提供了新參考。
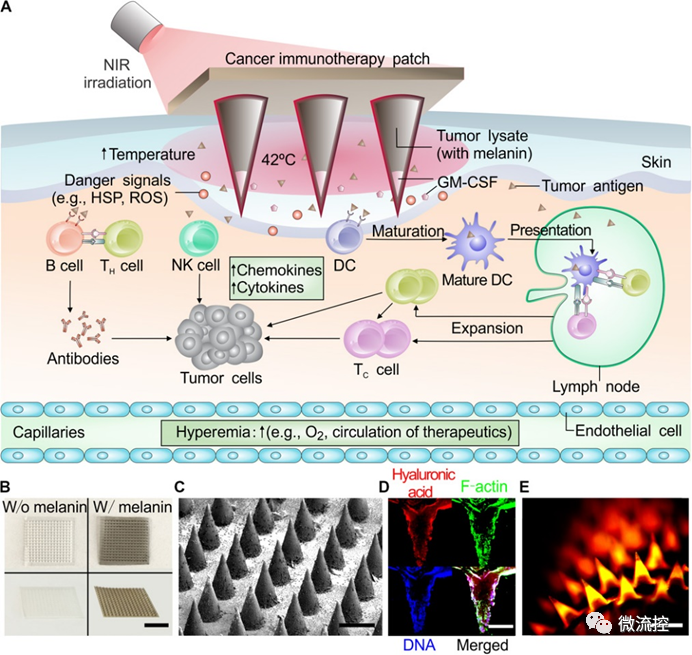
圖2 利用基于透皮微針的疫苗貼片進行黑色素介導的癌癥免疫治療
(2)表面涂覆游離抗原微針
將游離抗原通過浸漬或蘸取的方式涂覆在固體微針表面,可獲得涂層微針。相比實心微針省去了藥物涂抹步驟,操作更簡單快捷。同時通常利用靜電吸附作用將抗原、佐劑與針體相結合,提高微針的載藥量。Zeng等直接將陽離子精氨酸結構域修飾的酪氨酸相關蛋白2與胞嘧啶磷酸鳥苷寡脫氧核苷酸(CpG)寡核苷酸形成的電解質膜涂覆于聚丙交酯微針上。線性沉積的聚電解質膜多達128層,厚度約200 nm,載藥量超過225 μg/cm2。結果在小鼠模型中誘導了強烈的特異性免疫反應,并產生持久的免疫記憶。
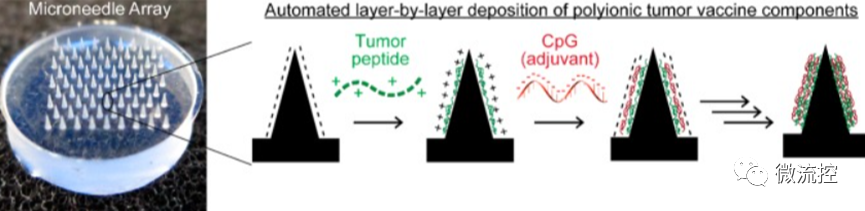
圖3 在微針陣列上涂覆免疫聚電解質多層膜以增強癌癥免疫
納米疫苗微針
納米疫苗微針是將腫瘤抗原首先封裝于納米顆粒中,如聚合物膠束、脂質體、納米復合物等,然后分散于微針針體中制備而得。利用微針系統穿透角質層,將載腫瘤抗原納米顆粒遞送至皮膚中,被樹突狀細胞攝取后激活腫瘤免疫作用。納米疫苗微針能增強抗原在淋巴結的蓄積,常包括以下機制:(1)10 nm ~ 100 nm的顆粒能夠穿過細胞外基質直接到達淋巴結;(2)納米顆粒可被皮膚部位的樹突狀細胞更高效地捕獲,并遷移至引流淋巴結;(3)在納米顆粒表面修飾與樹突狀細胞表面受體相識別的配體,能夠實現淋巴結的靶向遞送。Zhou等將CD40蛋白抗體(αCD40)修飾到載有卵清蛋白(OVA)、Poly I:C和派姆單抗的脂質體表面,然后封裝在透明質酸微針中。進入機體后,αCD40能靶向樹突狀細胞表面高度表達的CD40,進而激活樹突狀細胞的成熟,促進納米疫苗在淋巴結的蓄積,同時聯合派姆單抗,增強細胞毒性T細胞的活化,實現抗腫瘤免疫反應的增強和免疫抑制微環境向免疫激活的逆轉。
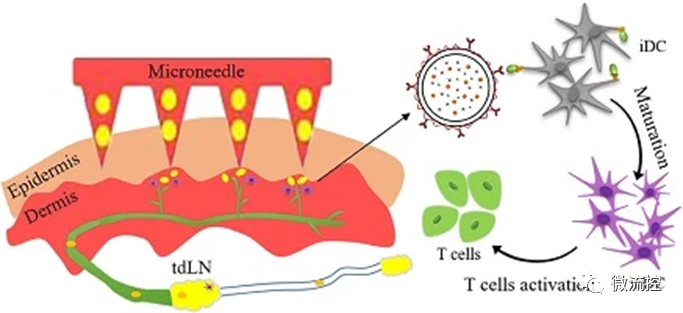
圖4 納米疫苗復合微針用于抗腫瘤免疫治療
樹突狀細胞疫苗微針
分離外周血自體樹突狀前體細胞,經細胞因子或抗原刺激和誘導生成成熟樹突狀細胞。制備的樹突狀細胞疫苗回輸至體內,能夠有效地抑制腫瘤,具有安全性高、免疫原性強等優點。利用微針遞送樹突狀細胞細胞,制備樹突狀細胞疫苗微針時,需要同時保證微針的機械強度和樹突狀細胞細胞的活力與釋放效率。由于細胞可以保存在低溫環境中,所以可以采用合適的低溫保護介質作為微針基質材料。例如,Hao等在維持樹突狀細胞細胞活力和保證微針脫模完整性的條件下,篩選出2.5%二甲基亞砜和100 mmol/L蔗糖的磷酸鹽緩沖溶液作為最佳低溫介質,并將預先懸浮的樹突狀細胞細胞置于微針模具中進行-20℃ ~ -196℃梯度冷卻,固化后制備得樹突狀細胞疫苗微針。結果顯示,從微針中釋放的樹突狀細胞細胞存活率達71.4% ± 1.4%,在液氮中保存1個月后活力不變。與靜脈注射和皮下注射樹突狀細胞疫苗相比,樹突狀細胞疫苗微針在小鼠體內產生更強的特異性免疫反應和更有效的腫瘤抑制能力。
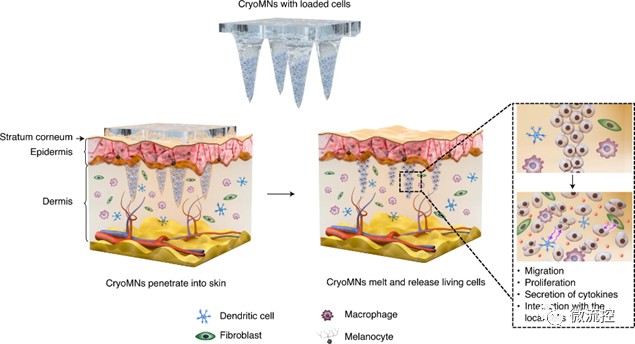
圖5 用于經皮遞送樹突狀細胞的低溫微針
總體而言,微針系統作為一種安全無毒、使用方便、能夠個體化皮下給藥的新模式,在腫瘤抗原的遞送中占有巨大優勢。然而,將疫苗微針用于更多的腫瘤類型、縮短實驗與臨床差距以及解決微針系統制造工藝、腫瘤疫苗的配方設計、生產儲運等問題,仍需進一步探索。相信在不久的未來,微針系統可以成為遞送腫瘤抗原的一個重要措施。
審核編輯:劉清
-
電解質
+關注
關注
6文章
813瀏覽量
20070
原文標題:綜述:微針系統在腫瘤疫苗中的研究進展
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
微流控技術在病原微生物檢測中的研究進展
高能點焊電源技術在現代工業制造中的應用與研究進展

使用原代腫瘤細胞進行藥物篩選的數字微流控系統
上海光機所在多路超短脈沖時空同步測量方面取得研究進展
AI大模型的最新研究進展
射頻功率放大器在腫瘤細胞表面EGFR研究中的應用
導熱紙(膜)的研究進展 | 晟鵬技術突破導熱芳綸紙

了解振弦采集儀在建筑物安全監測中的應用與研究

哈爾濱工業大學在微納光學領域取得重要進展

綜述:高性能銻化物中紅外半導體激光器研究進展

先進封裝中銅-銅低溫鍵合技術研究進展





 微針系統在腫瘤疫苗中的研究進展
微針系統在腫瘤疫苗中的研究進展












評論