基因治療是一類在疾病發(fā)生的最根本層面上實現(xiàn)相關(guān)治療的研究策略。現(xiàn)已上市的基因治療藥物大多是以病毒為載體實現(xiàn)基因遞送的。病毒載體的引入無疑會引起人們對該類治療體系的生物安全性產(chǎn)生顧慮。因此,發(fā)展生物相容的基因遞送載體就顯得越來越重要,并且成為具有挑戰(zhàn)性的前沿課題之一。近年來發(fā)展起來的DNA折紙納米技術(shù)是一種獨特的自下而上的自組裝納米技術(shù),可被用于設(shè)計和制備具有各類尺寸和形貌可控的自組裝納米結(jié)構(gòu)。DNA納米結(jié)構(gòu)和基因藥物具有化學(xué)組成上的一致性,在具有生物相容性的基因遞送載體的設(shè)計上表現(xiàn)出顯著的優(yōu)勢。
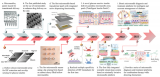
圖:DNA折紙結(jié)構(gòu)負載化療藥物和基因藥物,靶向耐藥腫瘤細胞,實現(xiàn)耐藥腫瘤生長抑制示意圖
2012年以來,中國科學(xué)院國家納米科學(xué)中心丁寶全課題組以自組裝的多功能核酸納米結(jié)構(gòu)為基礎(chǔ),構(gòu)建了一系列藥物遞送載體。所遞送的藥物組分涉及化療小分子藥物(J. Am. Chem. Soc.2012, 134, 13396;ACS Nano2014, 8, 6633)、光熱治療納米顆粒藥物(Small2015, 11, 5134;Adv. Mater.2016, 28, 10000)、功能性蛋白類藥物(Nat. Biotechnol.2018, 36, 258),以及核酸類藥物(ACS Appl. Mater. Interfaces2017, 9, 20324;Nano Lett.2018, 18, 3328)。該類多功能核酸納米藥物遞送體系表現(xiàn)出非常好的腫瘤靶向性和生物相容性,可作為全新的疾病診斷和治療平臺。在最近發(fā)表的研究工作中,丁寶全課題組首次利用DNA折紙結(jié)構(gòu)為載體高效且可控地實現(xiàn)了化療藥物阿霉素和線性小發(fā)卡RNA轉(zhuǎn)錄模板的共遞送,完成了化療和基因治療的聯(lián)合給藥。該研究成果以A Tailored DNA Nanoplatform for Synergistic RNAi-/Chemo- Therapy of Multidrug-Resistant Tumors為題被《德國應(yīng)用化學(xué)》雜志在線發(fā)表(Angew. Chem. Int. Ed.2018, DOI: 10.1002/anie.201809452)。
基因治療在癌癥治療領(lǐng)域的研究已經(jīng)被廣泛報道,大多是通過各類陽離子脂質(zhì)體、高分子聚合物和無機納米顆粒等為載體實現(xiàn)基因遞送。多功能DNA納米結(jié)構(gòu)作為一種生物相容的納米載體可以很好地應(yīng)用于基因類藥物的遞送研究。以靶向修飾的三角形DNA折紙結(jié)構(gòu)為載體,首先通過堿基間嵌插的方式實現(xiàn)化療藥物阿霉素的高效負載。隨后,利用核酸鏈間的堿基互補配對策略定點連接上靶向多藥耐藥相關(guān)基因(P糖蛋白和生存素)的線性小發(fā)卡RNA轉(zhuǎn)錄模板。該類化療藥物和基因藥物共負載的DNA納米給藥體系可通過修飾的核酸適配體實現(xiàn)對具有阿霉素耐藥性的乳腺癌腫瘤細胞靶向遞送。通過胞內(nèi)pH響應(yīng)和還原氛圍實現(xiàn)阿霉素和基因藥物的可控釋放,利用RNA干擾的方法實現(xiàn)P糖蛋白和生存素的表達下調(diào),達到對腫瘤細胞的殺傷。小鼠活體實驗結(jié)果表明,該類DNA納米給藥體系表現(xiàn)出非常好的腫瘤靶向性和生物相容性,能夠?qū)δ退幮匀橄侔┠[瘤模型產(chǎn)生顯著的治療效果。該研究基于生物系統(tǒng)的天然核酸結(jié)構(gòu),實現(xiàn)了化療和基因治療的聯(lián)合給藥,為惡性腫瘤等疾病的治療提供新的研究策略。
論文的第一作者是國家納米中心助理研究員劉建兵,通訊作者為丁寶全。該研究得到國家自然科學(xué)基金委員會和中科院前沿科學(xué)重點研究計劃等的支持。
-
納米技術(shù)
+關(guān)注
關(guān)注
2文章
201瀏覽量
25860 -
DNA
+關(guān)注
關(guān)注
0文章
243瀏覽量
31093
原文標題:國家納米中心利用核酸自組裝結(jié)構(gòu)實現(xiàn)基因藥物遞送
文章出處:【微信號:Microfluidics-Tech,微信公眾號:微流控科技】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
相關(guān)推薦
PCIe收發(fā)卡設(shè)計資料:611-基于VU9P的2路4Gsps AD 2路5G DA PCIe收發(fā)卡

基于漩渦湍流輔助的微流控平臺,可實現(xiàn)類精子結(jié)構(gòu)的微型機器人一步成型

半侵入式"可穿戴診所"——微針技術(shù)的創(chuàng)新應(yīng)用
小小發(fā)卡器 加密寫數(shù)據(jù)

可控硅輸出光耦的結(jié)構(gòu)和特性
DNA計算機研究取得突破性進展:PB級數(shù)據(jù)存儲與高效處理
信達生物利用AI技術(shù)為藥物研發(fā)插上翅膀
人員定位發(fā)卡機智能充電柜,集人臉識別發(fā)卡充電于一體
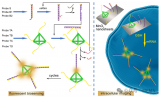
基于熵驅(qū)動鏈置換策略的高靈敏mRNA檢測與細胞內(nèi)成像研究




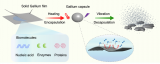
 首次利用DNA折紙結(jié)構(gòu)為載體高效且可控地實現(xiàn)了化療藥物阿霉素和線性小發(fā)卡RNA轉(zhuǎn)錄模板的共遞送
首次利用DNA折紙結(jié)構(gòu)為載體高效且可控地實現(xiàn)了化療藥物阿霉素和線性小發(fā)卡RNA轉(zhuǎn)錄模板的共遞送











評論