01 ? 導讀
在傳統可充電鋰離子電池(LIB)中,以碳酸亞乙酯(EC)為主的Li+初級溶劑化鞘(PSS)在Gr上能夠形成獨特的固體電解質界面(SEI),抑制溶劑的共嵌入,并避免Gr的結構坍塌。為了提高電池安全性,在EC基電解質中引入有機磷酸鹽作為共溶劑,可以增加電解液的阻燃性。
然而,大多數有機磷酸鹽表現出高的極性和強的給電子能力,可以與Li+配位。因此,磷酸鹽分子進入PSS并部分取代EC分子(圖1a)。通過這種方式,磷酸鹽參與了初級SEI的形成,并破壞了原來的SEI。此外,配位磷酸鹽傾向于與Li+共嵌入Gr晶格中。插層分子在低電位下的分解會使Gr顆粒破裂,并導致性能迅速下降。因此,在不干擾電極材料儲鋰性能的情況下構建阻燃電解質仍然具有挑戰性。
02 ? 成果背景
近日,JACS上發表了一篇題為“Noncoordinating Flame-Retardant Functional Electrolyte Solvents for Rechargeable Lithium-Ion Batteries”的文章,該文章提出了一種非配位阻燃共溶劑,能夠提高電池安全性,同時避免對儲鋰過程的干擾。選用具有良好理化性能的高效阻燃劑六氟環三磷腈作為共溶劑制備功能電解質。
給電子能力低的非極性磷腈分子不能與Li+配位,因此被排除在初級溶劑化鞘外。在基于石墨負極的鋰離子電池中,磷腈分子在充電過程中不會與鋰離子共插進入石墨晶格中,有助于保持負極結構和界面的完整性,實現穩定循環。
03 ? 關鍵創新
(1)六氟環三磷腈(HFP)作為一種非配位的阻燃共溶劑,不參與構建Li+溶劑化鞘,因此不會破壞原有的SEI結構。
(2)HFP不與Li+共插入石墨層間,因此避免了石墨負極結構和界面的破壞。
(3)HFP的高阻燃特性極大提高了電池安全性。
04 ? 核心內容解讀
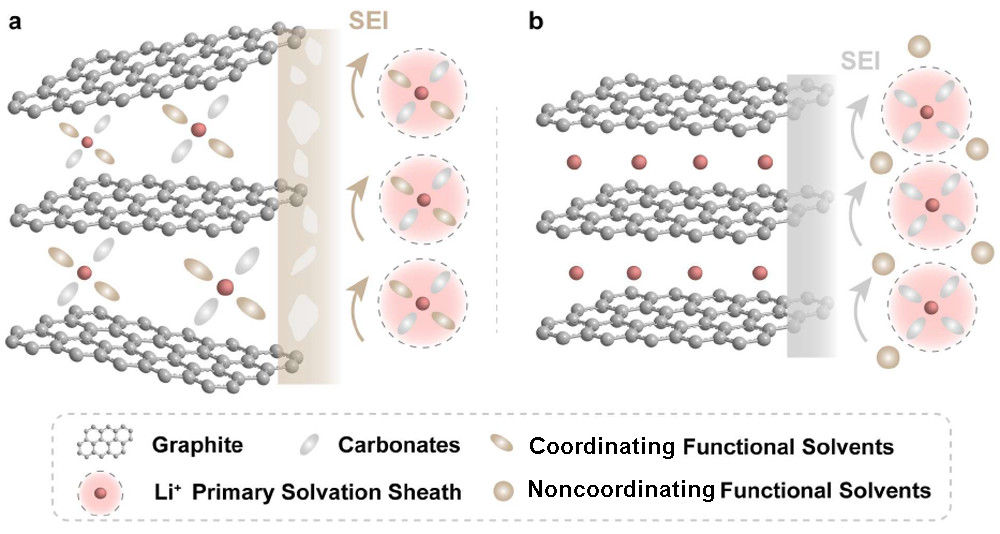
圖1.?在(a)具有配位共溶劑的電解質和(b)具有非配位共溶劑的電解質中,Li+嵌入Gr的示意圖。
本工作提出了一種新的非配位共溶劑——六氟環三磷腈(HCP),它可以提高電解質阻燃性,但對Li+溶劑化結構的影響最小(圖1b)。HCP是一種全氟六元芳族磷腈分子,作為阻燃共溶劑,被引入傳統的碳酸鹽電解質E1(0.8 M LiPF6?in?EC/碳酸二乙酯(DEC),1:1.5 m/m),獲得功能性電解質E2(0.8 M LiPF6?in EC/DEC/HCP,11 mm)。通過將經典的磷酸鹽TMP加入E1來制備電解質E3(0.8 M LiPF6?in EC/DEC/TMP,11 mm),并作為對照組。E1和E3可點燃并劇烈燃燒。相反,E2不能被點燃。
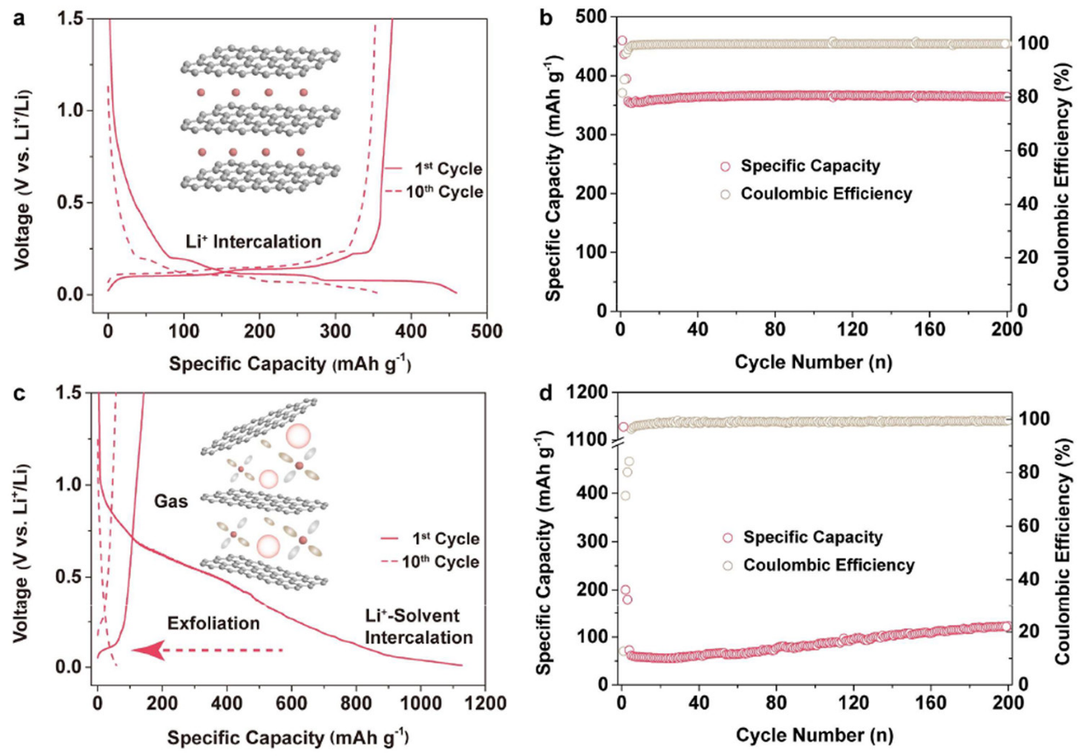
圖2.?使用(a, b)E2和(c, d)E3電解質的Li||Gr電池(a, c)恒流充放電曲線和(b, d)循環性能。
作為鋰離子電池最常用的負極材料,Gr對電解質和SEI有著嚴格的要求。為了研究上述電解質的電化學相容性,對Li||Gr電池進行了測試。在初始放電過程中,Li|E1|Gr和Li|E2|Gr電池的比容量均約為460 mAh g-1,具有三個電壓平臺,分別對應于SEI形成和Li+嵌入Gr(圖2a)。相比之下,Li|E3|Gr電池的比容量大于1000 mAh g-1,電壓曲線表明發生了大量溶劑共嵌入和分解(圖2c)。
Li|E1|Gr和Li|E2|Gr表現出穩定的循環性能,并在200次循環后,保持約100%的初始充電容量(圖2b),而Li|E3|Gr容量迅速下降(圖2d)。顯然,將HCP引入碳酸鹽電解質不會影響與Gr的相容性。
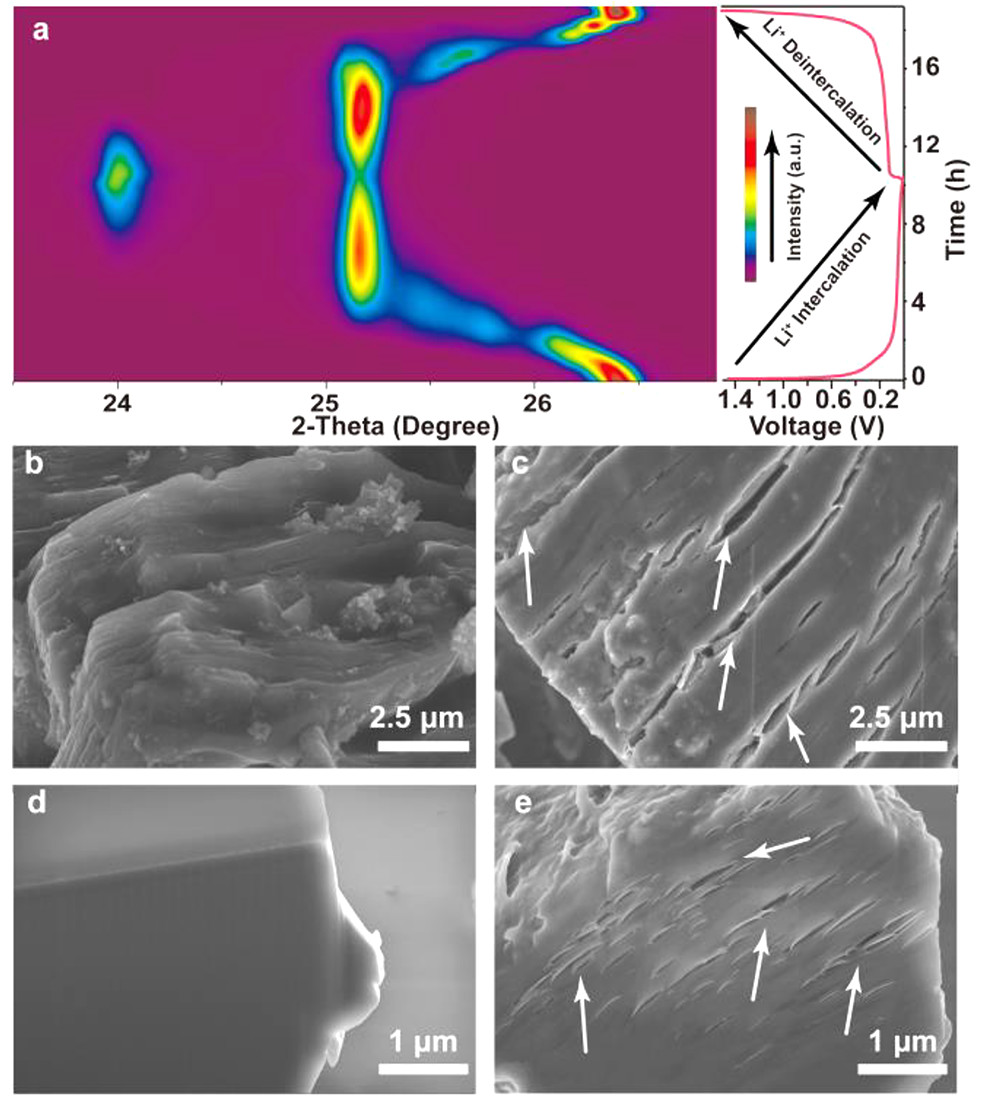
圖3.?Li|E2|Gr電池(a)第一次充放電循環(0.1C, 0.01-1.5 V)的原位XRD等高線圖。在(左)E2和(右)E3電解質中第一次循環后,Gr的(b, c)SEM圖和(d, e)FIB-SEM圖。@ACS
接下來,研究了在不同荷電狀態下Gr的X射線衍射(XRD)譜圖。Li|E2|Gr電池充放電過程的原位XRD譜圖(圖3a)顯示,Gr的(002)峰位置在Li+插層過程中由26.4°變為23.7°,放電過程中向相反方向對稱移動,表明Li+插層具有高的可逆性。SEM圖像顯示,在E3中循環后的Gr顆粒明顯膨脹,表面(圖3c)和內部(圖3e)均有明顯裂紋。
相反,E2(圖3b,d)中循環的Gr顆粒保持良好,沒有可見裂紋。這些明顯的裂紋和Gr在E3中的巨大徑向膨脹(約10倍)可能是由于共插的溶劑分子分解導致層狀結構剝落。
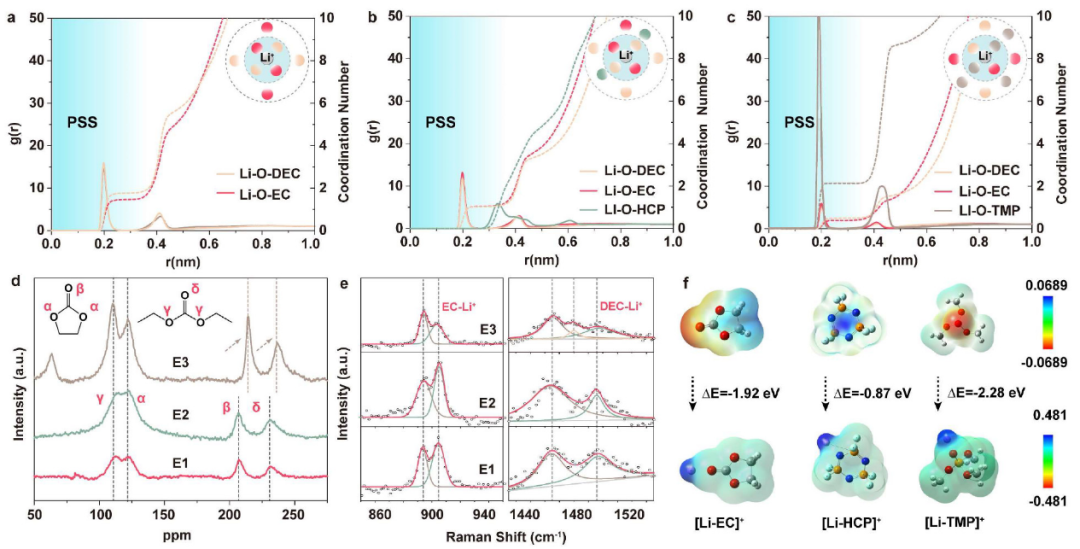
圖4.?(a-c)不同電解質的Li-O徑向分布函數。所附原理圖顯示了相應的溶劑化結構。不同電解質的(d)17O核磁共振譜和(e)拉曼光譜。(f)溶劑和溶劑化結構的靜電勢分布。@ACS
接下來,通過分子動力學(MD)模擬來說明Li+在不同電解質中的溶劑化結構(圖4a-c)。首先,對溶劑化層中與Li+相互作用的溶劑分子進行計數和平均。如圖4c所示,E3的Li+?PSS中存在TMP,平均配位數為2.13,遠遠大于EC和DEC的配位數(分別為0.39和0.49)。相比之下,HCP幾乎沒有參與PSS(r<3 ?),E2中的平均配位數接近于0(圖4b)。與E1的情況一樣(圖4a),由于HCP的非配位性,EC和DEC在E2的Li+?PSS中仍然占主導地位。
采用密度泛函理論(DFT)模擬計算溶劑和溶劑化結構的形成能和靜電勢(圖4f)。相對于HCP, TMP和EC具有更強的表面負電荷,表現出更強的給電子能力和Li+配位能力。[Li+-溶劑]形成能可定義為
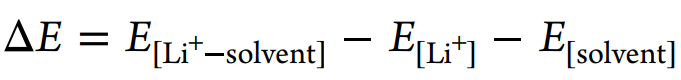
ΔE[Li+-EC](?1.92 eV)比ΔE[Li+-HCP](?0.87 eV)大得多,但小于ΔE[Li+TMP](?2.28 eV),說明這三種溶劑的配位能力為TMP>EC?HCP, HCP不能在熱力學上取代EC。
通過17O核磁共振光譜、拉曼光譜和電噴霧質譜(ESI-MS),進一步研究了電解質的溶劑化結構。如圖4d所示,EC和DEC中有兩組不等效的17O核,羰基17O(β和δ)位于200和250 ppm之間,醚17O(α和γ)位于75和150 ppm之間。E3中羰基17O核經歷了下場位移,脫屏蔽效應增強,這可能與TMP參與Li+?PSS以及Li+與碳酸鹽溶劑之間離子偶極相互作用減弱有關。
相反,E2中沒有發現位移,說明HCP不影響[Li+-碳酸鹽]的溶劑化結構。905 cm-1處的拉曼峰(圖4e)代表[Li+-EC]鍵。相對于E1, E3中905 cm-1處的峰強度明顯降低,而E2中無明顯變化。在1486 cm-1處的[Li+-DEC]峰也可以觀察到類似的結果。這表明HCP對碳酸鹽的溶劑化狀態影響較弱,證實了其非配位性。
05 ? 成果啟示
本工作提出了一種非配位的磷腈共溶劑,以提高電解質的阻燃性,同時避免干擾LIBs中的電荷轉移和存儲過程。與傳統的有機磷酸鹽不同,非配位HCP分子不參與Li+?PSS的形成,也不與Li+共插到負極結構中,因此不會導致負極-電解質界面退化或SEI不穩定。基于該新型電解質的LIB具有良好的循環性能。該新型非配位阻燃共溶劑與其他正極穩定劑結合,有望協同提高可充電電池的存儲和安全性能,在未來的電化學系統中具有廣闊的應用前景。
審核編輯:劉清
